Concentração Micelar Crítica (CMC): O que é, como funciona e aplicações
A Concentração Micelar Crítica (CMC) é a concentração exata de surfactantes em uma solução a partir da qual as moléculas deixam de estar dispersas individualmente e passam a formar agregados organizados chamados micelas . Esse parâmetro é o divisor de águas na físico-química de superfícies: abaixo da CMC, o surfactante apenas reduz a tensão superficial; acima dela, o sistema ganha a capacidade de solubilizar gorduras e óleos dentro do núcleo hidrofóbico das micelas formadas.
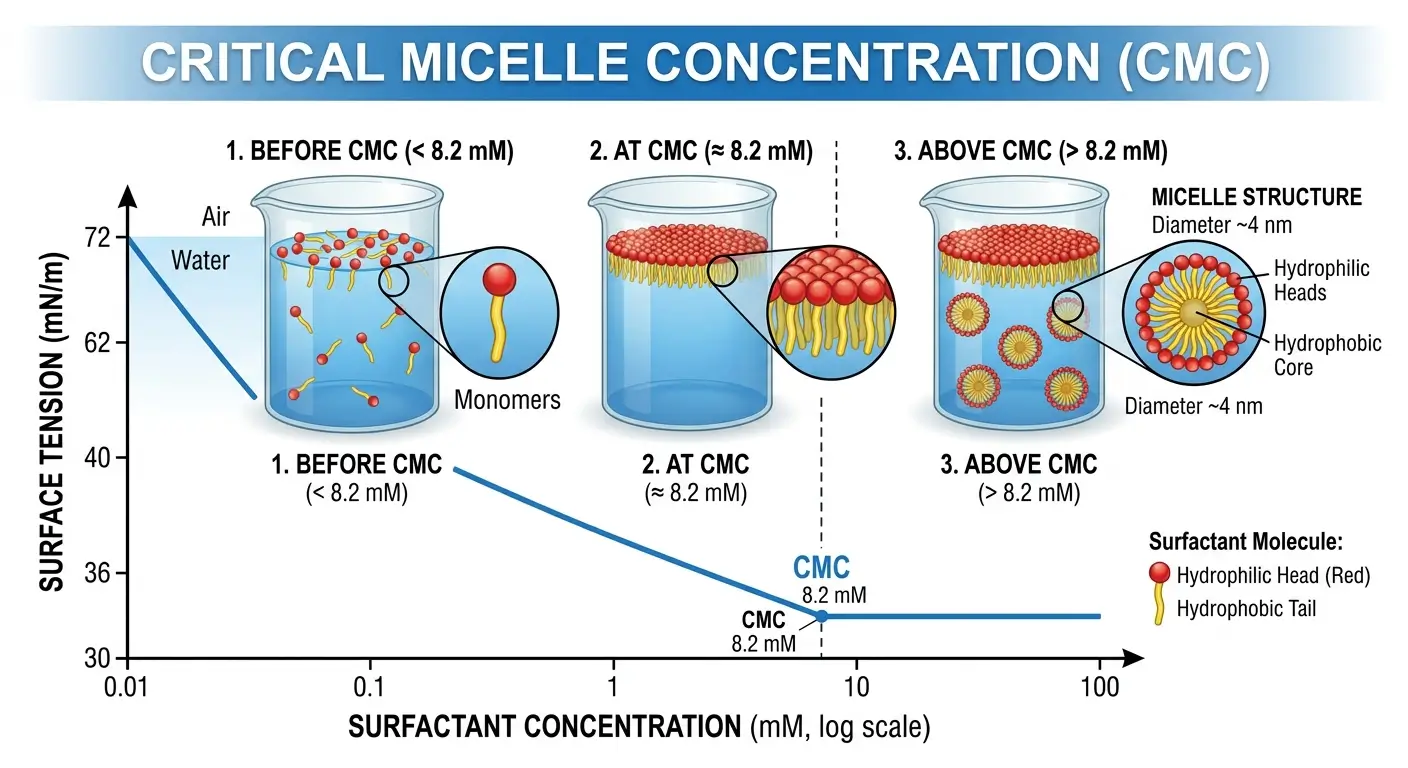
O que é a Concentração Micelar Crítica (CMC)?
A CMC define o momento exato em que uma solução contendo agentes tensoativos muda seu comportamento físico. É o limite de concentração onde as moléculas deixam de atuar apenas individualmente e passam a formar estruturas organizadas.
Definição técnica e significado do símbolo
Tecnicamente, a CMC é a concentração de surfactantes acima da qual as micelas se formam espontaneamente. O símbolo universal é o acrônimo CMC .
Antes desse ponto, o soluto encontra-se disperso como monômeros. Após esse valor, quase todo surfactante adicional inserido no sistema se converterá em novas micelas.
O papel dos surfactantes (tensoativos) na solução
Os surfactantes são moléculas anfifílicas , possuindo uma porção hidrofílica (cabeça polar) e uma hidrofóbica (cauda apolar). Em solução aquosa, essas moléculas migram para as interfaces para evitar o contato das caudas com a água.
Consequentemente, elas reduzem a tensão superficial do líquido. Isso facilita processos essenciais como a molhagem, a dispersão e a emulsificação de óleos.
Como se formam as micelas? O processo passo a passo
A formação micelar é um fenômeno de auto-organização impulsionado pela termodinâmica. Para entender como a CMC ocorre, devemos observar o comportamento das moléculas em diferentes estágios de concentração.
Comportamento dos surfactantes abaixo da CMC (Adsorção na interface)
Em concentrações muito baixas, os monômeros de surfactante estão dispersos ou adsorvidos na superfície (interface ar-água). Nesse estágio, cada molécula adicionada reduz drasticamente a tensão superficial.
Além disso, as propriedades físicas da solução, como a condutividade e a pressão osmótica, variam de forma linear. A variação é diretamente proporcional à quantidade de soluto adicionada ao meio.
O ponto de saturação: O que acontece exatamente no valor da CMC?
Quando a interface fica completamente saturada de moléculas, o sistema atinge o ponto de CMC. A partir daqui, a tensão superficial torna-se praticamente constante.
O sistema não consegue mais acomodar monômeros na superfície. Isso força as moléculas a se agruparem no seio do líquido para proteger suas caudas hidrofóbicas do contato desfavorável com o solvente.
Estrutura das micelas esféricas e a termodinâmica
As micelas esféricas são os primeiros agregados a surgir. Elas se organizam com as caudas voltadas para o centro (núcleo hidrofóbico) e as cabeças voltadas para fora.
Esse processo é impulsionado pelo efeito hidrofóbico . Ocorre um ganho de entropia no sistema, pois as moléculas de água são liberadas das estruturas ordenadas que formavam ao redor das caudas individuais. Portanto, a micelização é um processo energeticamente favorável.
Como determinar a CMC (Principais Métodos Experimentais)
A determinação precisa da CMC é essencial para o controle de qualidade industrial. Diversos métodos monitoram a mudança súbita nas propriedades físicas da solução.
O método clássico: Gráfico de Tensão Superficial × log[Concentração]
Este é o método mais comum na literatura. Mede-se a tensão superficial em função do logaritmo da concentração. O gráfico apresenta uma queda linear até a CMC.
Nesse ponto, ocorre uma quebra brusca (inflexão) na curva. Os valores permanecem constantes após esse ponto, indicando que a superfície atingiu sua saturação máxima.
Condutividade Elétrica: Identificando a CMC em surfactantes iônicos
Para tensoativos carregados, como o SDS, a condutividade elétrica é o método ideal. Antes da CMC, a condutividade sobe rapidamente de forma linear.
No entanto, após a formação das micelas, a taxa de aumento diminui. Isso ocorre devido à menor mobilidade das micelas e ao aprisionamento de contra-íons em sua dupla camada elétrica.
Espectroscopia e Fluorescência: Solubilização de corantes hidrofóbicos
Este método utiliza sondas químicas (como o pireno) que mudam sua fluorescência ao entrarem em ambientes apolares.
Quando as micelas surgem, o corante migra para o seu interior hidrofóbico. Isso gera um sinal óptico detectável que marca com precisão o valor da CMC no experimento.
Métodos complementares: Espalhamento de luz (DLS), Pressão Osmótica e Turbidimetria
Técnicas como o DLS (Dynamic Light Scattering) detectam o aparecimento de partículas nanométricas na solução.
Já a turbidimetria observa mudanças na clareza da solução. Ao mesmo tempo, a pressão osmótica indica a redução do número de partículas livres devido ao processo de agregação molecular.
Fatores que influenciam o valor da Concentração Micelar Crítica
A CMC não é uma constante fixa; ela depende diretamente da arquitetura molecular e das condições do solvente.
Efeito da cadeia hidrofóbica: O comprimento da cauda de carbono
Quanto maior a cadeia de carbono da cauda, menor será a CMC. Em geral, para surfactantes iônicos, a CMC diminui pela metade a cada dois carbonos adicionados à cauda.
Isso acontece porque cadeias longas são mais instáveis em meio aquoso. Consequentemente, o sistema favorece a agregação precoce para estabilizar as cadeias apolares.
Natureza da cabeça polar: Diferenças entre surfactantes iônicos e não iônicos
Surfactantes não iônicos possuem CMCs significativamente menores que os iônicos. O motivo principal é a ausência de repulsão eletrostática entre as cabeças polares.
Em contrapartida, nos iônicos, as cabeças de mesma carga se repelem. Isso dificulta a aproximação das moléculas e exige uma concentração maior para forçar a formação da micela.
Influência de eletrólitos e força iônica (Efeito de Salting-out)
A adição de sais (eletrólitos) reduz a CMC de surfactantes iônicos. O sal "blinda" as cargas das cabeças polares, diminuindo a força de repulsão entre elas. Dessa forma, as micelas conseguem se formar com concentrações muito menores de tensoativo no meio.
Variáveis ambientais: Temperatura (Ponto Krafft) e solventes orgânicos
A temperatura afeta a hidratação das cabeças polares. Para surfactantes como o SDS, a CMC apresenta um mínimo em torno de 25–30°C, aumentando ligeiramente acima disso.
Além disso, existe o Ponto Krafft , a temperatura mínima necessária para que a formação de micelas seja possível. Já os solventes orgânicos costumam aumentar a CMC por tornarem o meio menos polar.
Diferença entre CMC e outros conceitos de agregação
CMC vs. CAC (Concentração de Agregação Crítica em polímeros)
Enquanto a CMC é intrínseca ao surfactante puro, a CAC ocorre na interação com polímeros. Geralmente, a CAC é muito menor que a CMC. As cadeias poliméricas facilitam o agrupamento das moléculas de surfactante ao longo de sua estrutura.
Comportamento da CMC em misturas de surfactantes (Sinergia)
Em formulações comerciais, misturas de diferentes tensoativos costumam apresentar uma CMC experimental menor que a média dos componentes puros. Esse efeito de sinergia é amplamente explorado para reduzir custos e aumentar a performance dos produtos.
Importância e Aplicações Práticas da CMC
Higiene, Cosméticos e Farmacologia
A limpeza eficaz só ocorre acima da CMC, quando as micelas conseguem "encapsular" as sujeiras gordurosas. Na estética, a água micelar utiliza micelas para atrair impurezas sem agredir a pele.
Na medicina, as micelas atuam no drug delivery . Elas transportam fármacos hidrofóbicos pelo organismo, liberando-os de forma controlada no alvo terapêutico.
Perguntas Frequentes sobre CMC (FAQ)
-
Qual é o valor típico de CMC do SDS (Dodecil Sulfato de Sódio)?
-
- Para o SDS puro em água a 25°C, a literatura reporta valores entre 8,1 e 8,2 mM (milimolar). Variações leves podem ocorrer dependendo da pureza do reagente e do método de medição.
-
-
Por que a tensão superficial para de cair bruscamente após a CMC?
-
- Porque a interface ar-água já está totalmente saturada. Novas moléculas adicionadas preferem formar micelas no seio do líquido em vez de se posicionarem na superfície já ocupada.
-
-
A CMC aumenta ou diminui com o aumento da temperatura?
-
- O comportamento costuma seguir uma forma de "U". Para muitos iônicos, ela diminui até um ponto mínimo (próximo à temperatura ambiente) e volta a subir ligeiramente com o calor.
-
-
O que acontece se a concentração estiver abaixo da CMC?
-
- A solução terá apenas monômeros individuais. Nesse estado, o sistema não possui capacidade de solubilizar gorduras ou óleos de forma eficiente.
Tabela de Referência Rápida (Valores Médios)
| Surfactante | Tipo | CMC Aproximada (25°C) |
|---|---|---|
| SDS | Aniônico | 8,1 – 8,2 mM |
| CTAB | Catiônico | 0,9 – 1,0 mM |
| Triton X-100 | Não iônico | 0,2 – 0,3 mM |











