O Que Esperar no Mercado Farmacêutico Brasileiro em 2026
A prazo de expiração da patente da semaglutida , princípio ativo do Ozempic e Rybelsus, ocorre em 20 de março de 2026, e foi confirmada por decisão unânime do Superior Tribunal de Justiça (STJ) em dezembro de 2025, abrindo caminho para versões genéricas, similares e biossimilares.

O mercado de agonistas de GLP-1 no Brasil atingiu cerca de R$ 11 bilhões em 2025 . As importações de medicamentos como Ozempic e Mounjaro somaram US$ 1,669 bilhão — um salto de 88% comparado a 2024 . Com a entrada de genéricos, analistas projetam que esse mercado alcance R$ 20 bilhões já em 2026 e potencialmente R$ 50 bilhões até 2030 .
Neste artigo, você encontrará informações sobre:
- Impactos da queda da patente para a indústria farmacêutica
- Projeções de preços e acesso ampliado ao tratamento
- Análise detalhada do mercado pós-patente
- Empresas brasileiras que já se movimentam para produção local
- Equipamentos essenciais para P&D e controle de qualidade
- Requisitos regulatórios da Anvisa para aprovação
O Que é a Semaglutida e Por Que a Patente É Tão Importante
A semaglutida é um análogo do hormônio GLP-1 (peptídeo semelhante ao glucagon-1), desenvolvido pela Novo Nordisk para tratamento de diabetes tipo 2 e, posteriormente, aprovado para controle de obesidade. O medicamento atua estimulando a secreção de insulina, reduzindo o apetite e promovendo saciedade prolongada.
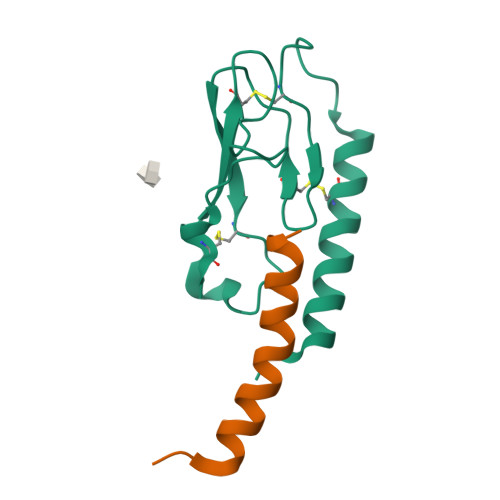
Representação visual do GLP-1. Fonte: https://www.rcsb.org/structure/3IOL
A patente concedia à Novo Nordisk exclusividade na produção e comercialização da semaglutida no Brasil desde 2006, impedindo que outros laboratórios fabricassem versões genéricas ou similares.
Com o fim dessa proteção em março de 2026, qualquer empresa farmacêutica que atenda aos requisitos regulatórios da Anvisa poderá produzir e comercializar medicamentos à base de semaglutida. Isso inclui genéricos sintéticos, similares e biossimilares — cada categoria com exigências específicas de bioequivalência e conformidade.
Impactos da Queda da Patente da Semaglutida no Brasil
A abertura do mercado para produção genérica traz consequências significativas para toda a cadeia farmacêutica brasileira. Com o fim da exclusividade da Novo Nordisk, o cenário competitivo se transforma completamente.
Produção Nacional e Redução de Dependência Externa
Atualmente, o Brasil importa a totalidade da semaglutida consumida no país. Com a queda da patente, laboratórios nacionais podem iniciar produção local, reduzindo a dependência de importação e fortalecendo a indústria farmacêutica brasileira. Empresas como EMS já investiram mais de R$ 1 bilhão em plantas industriais capazes de produzir do insumo ativo ao produto final.
Concorrência e Pressão nos Preços
A entrada de múltiplos concorrentes no mercado pressiona os preços para baixo. Por regulamentação, genéricos devem custar pelo menos 35% menos que o medicamento de referência. Na prática, a experiência brasileira mostra que reduções frequentemente superam 50% a 60% após os primeiros anos de competição.
O Ozempic original é comercializado por valores entre R$ 1.000 e R$ 1.300 por caneta. Com genéricos, estima-se que o custo mensal caia para R$ 400 a R$ 650, ampliando significativamente o acesso ao tratamento.
Ampliação do Acesso via SUS e Planos de Saúde
Preços mais acessíveis viabilizam a inclusão da semaglutida em protocolos do Sistema Único de Saúde (SUS) e ampliam a cobertura por planos de saúde. Isso beneficia milhões de brasileiros com diabetes tipo 2 e obesidade que atualmente não conseguem arcar com o tratamento.
Análise do Mercado de Semaglutida Pós-Patente
O segmento de análogos de GLP-1 apresenta crescimento explosivo no Brasil, impulsionado tanto pelo uso aprovado para diabetes quanto pela prescrição off-label para emagrecimento. Compreender as dimensões desse mercado é fundamental para laboratórios e profissionais do setor.
Números do Mercado Atual
Em 2023, o Ozempic registrou faturamento de R$ 3,1 bilhões — o maior valor anual para um único medicamento no país. Considerando todo o portfólio de semaglutida da Novo Nordisk, as vendas no mercado privado atingiram R$ 3,7 bilhões, com crescimento de 52% sobre o ano anterior.
O mercado de GLP-1 como um todo alcançou aproximadamente R$ 11 bilhões em 2025 . As importações anuais cresceram 82% nesse período, refletindo demanda aquecida que supera a capacidade de abastecimento.
Projeções Para os Próximos Anos
Analistas do setor farmacêutico projetam cenários otimistas para o mercado brasileiro de semaglutida:
- 2026: Mercado estimado em R$ 20 bilhões , com entrada dos primeiros genéricos e similares a partir de abril/maio
- 2028: Consolidação da produção nacional e maior penetração em faixas de renda média
- 2030: Potencial de R$ 50 bilhões , com cerca de 15 milhões de usuários e crescimento anual médio de 40%
Esses números representam oportunidade estratégica para laboratórios que se posicionarem adequadamente antes da expiração da patente.
Empresas Brasileiras Que Já Se Movimentam Para o Mercado Pós-Patente
A corrida pela fatia do mercado de semaglutida começou bem antes da decisão final do STJ. Diversas farmacêuticas brasileiras e internacionais aceleraram investimentos, parcerias e submissões de pedidos de registro à Anvisa. Até janeiro de 2026, a agência já havia recebido 13 pedidos de registro para medicamentos à base de semaglutida.
EMS: Investimento Bilionário em Produção Verticalizada
A EMS, líder no segmento de genéricos no Brasil, investiu mais de R$ 1 bilhão em sua nova fábrica em Hortolândia (SP) , inaugurada em 2025. A planta possui capacidade para produzir do insumo farmacêutico ativo ao produto final, garantindo verticalização completa. A empresa já realizou lançamentos com liraglutida (análogo de GLP-1) e planeja entrada imediata no mercado pós-patente da semaglutida.
Biomm: Parceria Internacional Para Biossimilar
A Biomm fechou acordo exclusivo com a indiana Biocon para distribuir e comercializar um biossimilar da semaglutida a partir de 2026. A empresa já protocolou pedido de registro na Anvisa e investiu em sua unidade de Nova Lima (MG) para produção de biossimilares de alta complexidade.
Hypera Pharma: Preparação Estratégica
A Hypera Pharma declarou preparação ativa para incluir semaglutida em seu portfólio logo após a expiração da patente. Com histórico de agilidade em lançamentos pós-patente — como rivaroxabana e apixabana — a empresa enxerga o segmento de GLP-1 como oportunidade de diversificação.
Prati-Donaduzzi: Pesquisa Avançada em Genérico
A Prati-Donaduzzi iniciou pesquisas avançadas para desenvolvimento de genérico da semaglutida, com importação de matéria-prima da Ásia e negociação de dispositivos de aplicação na Europa. A empresa está em fase de formulação e análise de resultados, com previsão de lançamento em 2026.
Cimed: Foco em Acessibilidade
A Cimed anunciou planos explícitos para produzir genéricos da semaglutida com intenção de lançamento imediato após a queda da patente. " Queremos ter uma canetinha amarela o mais rápido possível”, disse João Adibe, CEO da Cimed ao InfoMoney . A estratégia integra a expansão da empresa para receita bilionária, com ênfase em tornar o tratamento acessível.
A Anvisa publicou edital em agosto de 2025 priorizando análises de pedidos para produção nacional, o que acelera aprovações e favorece laboratórios brasileiros na corrida pelo mercado.
Requisitos Regulatórios da Anvisa Para Aprovação
O desenvolvimento e produção de genéricos ou biossimilares de semaglutida exige conformidade rigorosa com normas regulatórias brasileiras e internacionais. Laboratórios interessados devem atender a múltiplos requisitos para obter aprovação da Anvisa.
Exigências Para Genéricos Sintéticos
Medicamentos genéricos devem demonstrar bioequivalência ao produto de referência, comprovando que apresentam a mesma biodisponibilidade e eficácia terapêutica. As exigências incluem estudos clínicos comparativos, validação de processos de fabricação e conformidade com Boas Práticas de Fabricação (BPF) segundo a RDC 301/2019 .
Requisitos Para Produtos Injetáveis Estéreis
A semaglutida é comercializada como injetável subcutâneo, o que adiciona complexidade regulatória. Produtos estéreis devem atender ao Anexo 1 do EU GMP (Boas Práticas de Fabricação da União Europeia), com controles rigorosos de contaminação, partículas e esterilidade.
Conformidade com Normas de Salas Limpas
A produção de injetáveis exige ambientes classificados conforme ISO 14644 para salas limpas. O monitoramento contínuo de partículas viáveis e não viáveis é obrigatório para evitar contaminação.
Equipamentos Essenciais Para P&D e Controle de Qualidade
O desenvolvimento e produção de biossimilares ou genéricos de semaglutida exigem fases rigorosas: caracterização da molécula, formulação, escala-up, produção asséptica e controle de qualidade contínuo. Equipamentos de precisão são fundamentais para garantir conformidade regulatória e qualidade do produto final.
Fase de P&D e Desenvolvimento Analítico
A etapa inicial foca em análise de tamanho de partículas , potencial zeta , morfologia, estabilidade coloidal e dispersão. Para peptídeos como semaglutida, esses parâmetros são cruciais para garantir bioequivalência e otimizar a formulação injetável.

Analisador de Tamanho de Partículas LS 13320 XR da Beckman Coulter
Equipamentos recomendados para esta fase incluem analisadores de difração a laser como o Beckman Coulter LS 13 320 XR , sistemas de contagem e análise de tamanho como Beckman Coulter Multisizer 4e , e equipamentos de análise de nanopartículas via NTA como Particle Metrix ZetaView .
 Nova Geração em Análise de Nanopartículas
Nova Geração em Análise de Nanopartículas
Fase de Produção e Escala-up
A transição para produção em escala requer otimização de processos biotecnológicos com monitoramento em tempo real. Equipamentos como Beckman Coulter Vi-Cell Blu para análise automatizada de viabilidade celular e BioLector XT para cultivo microbiano otimizado são essenciais nesta etapa.
Controle de Qualidade e Monitoramento Ambiental
O monitoramento contínuo de partículas em salas limpas e áreas estéreis é obrigatório para produção de injetáveis. A série MET ONE da Beckman Coulter oferece contadores de partículas no ar para monitoramento remoto e contínuo em conformidade com ISO 14644 e EU GMP Anexo 1.
A preparação antecipada com infraestrutura adequada é chave para lançar produtos competitivos logo após março de 2026, reduzindo time-to-market e capturando participação de mercado.
Desafios da Produção de Semaglutida Genérica
Apesar das oportunidades, a produção de semaglutida apresenta desafios técnicos significativos que diferenciam este medicamento de genéricos convencionais.
Complexidade da Molécula
A semaglutida é um peptídeo de 31 aminoácidos com modificações estruturais que aumentam sua meia-vida no organismo. A síntese dessa molécula exige expertise em química de peptídeos e controles rigorosos de qualidade para garantir identidade, pureza e potência.
Formulação Injetável Estéril
O formato de caneta pré-preenchida adiciona complexidade ao processo produtivo. A formulação deve garantir estabilidade da molécula ao longo do prazo de validade, compatibilidade com o dispositivo de aplicação e esterilidade absoluta.
Cadeia de Suprimentos
A dependência de matérias-primas importadas representa vulnerabilidade para produtores locais. Garantir abastecimento consistente de insumos farmacêuticos ativos de qualidade é desafio logístico que impacta custos e capacidade produtiva.
Perspectivas Para Pacientes e Profissionais de Saúde
A queda da patente da semaglutida beneficia diretamente milhões de brasileiros que convivem com diabetes tipo 2 e obesidade. A ampliação do acesso ao tratamento pode impactar positivamente indicadores de saúde pública.
Maior Acessibilidade Econômica
Com preços reduzidos, pacientes que atualmente não conseguem arcar com o tratamento poderão iniciar ou manter o uso de semaglutida. Isso é particularmente relevante considerando que diabetes e obesidade afetam desproporcionalmente populações de menor renda.
Potencial Inclusão no SUS
Preços mais baixos viabilizam a avaliação de inclusão da semaglutida em protocolos clínicos do Sistema Único de Saúde. A Comissão Nacional de Incorporação de Tecnologias ( Conitec ) poderá reavaliar a relação custo-efetividade do medicamento com base nos novos valores de mercado.
Orientação Médica Continua Essencial
Independentemente da origem do medicamento — seja o produto de referência ou versões genéricas — o acompanhamento médico permanece fundamental. A semaglutida requer prescrição médica e monitoramento de efeitos adversos, ajuste de dose e avaliação de eficácia terapêutica.
FAQ: Perguntas Frequentes Sobre a Queda da Patente do Ozempic
Quando exatamente expira a patente da semaglutida no Brasil?
A patente expira em 20 de março de 2026, conforme decisão unânime do Superior Tribunal de Justiça (STJ) em dezembro de 2025, que rejeitou o pedido de extensão da Novo Nordisk.
Os genéricos terão a mesma eficácia que o Ozempic original?
Sim. Para obter registro na Anvisa, genéricos devem demonstrar bioequivalência ao produto de referência, comprovando mesma biodisponibilidade e eficácia terapêutica através de estudos clínicos comparativos.
Quanto devem custar os genéricos de semaglutida?
Por regulamentação, genéricos devem custar pelo menos 35% menos que o medicamento de referência. Na prática, espera-se que o custo mensal caia de R$ 1.000-1.300 para R$ 400-650 após a entrada de múltiplos concorrentes.
Quais empresas brasileiras vão produzir semaglutida genérica?
Entre as principais estão EMS, Biomm, Hypera Pharma, Prati-Donaduzzi e Cimed. A Anvisa já recebeu 13 pedidos de registro até janeiro de 2026.
A semaglutida genérica estará disponível pelo SUS?
Ainda não há confirmação, mas preços mais acessíveis viabilizam reavaliação pela Conitec. A inclusão dependerá de análise de custo-efetividade e decisão do Ministério da Saúde.
Qual a diferença entre genérico, similar e biossimilar de semaglutida?
Genéricos são cópias idênticas de medicamentos sintéticos. Similares passam por testes de bioequivalência mas podem ter excipientes diferentes. Biossimilares são versões de medicamentos biológicos que demonstram alta similaridade ao produto de referência.
Quando os primeiros genéricos devem chegar ao mercado?
A expectativa é que os primeiros genéricos e similares estejam disponíveis a partir de abril ou maio de 2026, considerando o tempo necessário para aprovação final e escala de produção após a expiração da patente.
Conclusão: Oportunidades e Preparação Para o Mercado Pós-Patente
A queda da patente da semaglutida representa marco transformador para o mercado farmacêutico brasileiro. Com projeções de crescimento para R$ 20 bilhões em 2026 e potencial de R$ 50 bilhões até 2030, o segmento de agonistas de GLP-1 oferece oportunidades significativas para laboratórios preparados.
A competição beneficia pacientes através de preços mais acessíveis e maior disponibilidade de tratamento para diabetes tipo 2 e obesidade. Para a indústria, representa oportunidade de fortalecer produção nacional, reduzir dependência de importação e capturar participação em mercado de alto crescimento.
Laboratórios que investirem antecipadamente em infraestrutura de P&D, controle de qualidade e conformidade regulatória estarão melhor posicionados para aproveitar essa janela de oportunidade a partir de março de 2026. Fale com a Dafratec e mantenha seu laboratório atualizado com os melhores equipamentos para análise laboratorial do mercado.