O isolamento de vesículas extracelulares (EVs) a partir do plasma representa uma das etapas mais críticas, e mais desafiadoras, da pesquisa biomédica contemporânea microtubulos. Estudos recentes demonstraram que o EXODUS supera métodos convencionais como ultracentrifugação (UC) e precipitação por polietilenoglicol (PEG), alcançando pureza mais de três vezes superior e rendimento 50 vezes maior a partir de apenas 20 µL de plasma.
Esses resultados redefinem o padrão técnico esperado para isolamento de EVs, com implicações diretas para a validade de análises proteômicas, transcriptômicas e ensaios funcionais downstream.
O mercado global de vesículas extracelulares tem apresentado expansão consistente, impulsionado pelo avanço das pesquisas em diagnóstico líquido, oncologia e desenvolvimento de terapias baseadas em EVs, refletindo a demanda crescente por métodos de isolamento reprodutíveis e escaláveis.
- Como o EXODUS isola vesículas extracelulares do plasma
- Resultados experimentais com o EXODUS H-600: TEM, rendimento e pureza
- Resultados experimentais com o EXODUS T-2800: TEM, Western blot e NTA
- H-600 vs. T-2800: quando usar cada modelo
- Aplicações em pesquisa biomédica e diagnóstico
O que são vesículas extracelulares e por que seu isolamento é desafiador
Vesículas extracelulares são estruturas lipoproteicas nanométricas liberadas por praticamente todos os tipos celulares, atuando como mediadores essenciais da comunicação intercelular. No plasma, carregam proteínas, ácidos nucleicos e lipídeos que refletem o estado funcional da célula de origem, o que as torna altamente relevantes para pesquisa biomédica e desenvolvimento de biomarcadores. A International Society for Extracellular Vesicles (ISEV) estabelece as diretrizes internacionais para nomenclatura, isolamento e caracterização dessas partículas.
No plasma, as EVs coexistem com proteínas do hospedeiro, lipoproteínas e debris celulares, todos na mesma faixa de tamanho e densidade. Quatro critérios definem a qualidade do isolamento:
- Pureza: remoção de proteínas co-isoladas e impurezas.
- Rendimento: quantidade de partículas recuperadas em relação ao total da amostra.
- Integridade: preservação da morfologia e atividade biológica.
- Reprodutibilidade: consistência entre operadores, amostras e escalas.
Métodos como ultracentrifugação (UC) e precipitação por polietilenoglicol (PEG) são amplamente utilizados, mas apresentam limitações conhecidas em pureza, tempo de processamento e risco de dano estrutural por cisalhamento elevado. Veja mais em Dilsiz (2024).
Como o EXODUS isola vesículas extracelulares do plasma
O EXODUS opera por nanofiltração de membrana dupla integrada a dois mecanismos de oscilação simultâneos. A oscilação de pressão negativa periódica (NPO) mobiliza o fluido na interface da membrana, prevenindo fouling. As oscilações harmônicas ultrassônicas duplamente acopladas (HO) mantêm as partículas em suspensão homogênea, prevenindo agregação.
Por meio de uma membrana nanoporosa, os exossomos são interceptados com precisão enquanto ácidos nucleicos livres e proteínas atravessam a membrana e são eliminados. O resultado é um isolamento altamente seletivo com baixo cisalhamento, preservando estrutura e função das partículas.
Esse princípio se aplica tanto ao H-600 (modelo compacto de bancada para volumes menores a médios) quanto ao T-2800 (sistema de grande escala para produção em larga escala e manufatura GMP).
Isolamento de EVs Plasmáticas com o EXODUS H-600: Resultados Experimentais
Os dados foram documentados pela Exodus Bio utilizando plasma de pacientes com carcinoma de células escamosas do esôfago, uma matriz complexa que representa condição clínica relevante para validação do método.

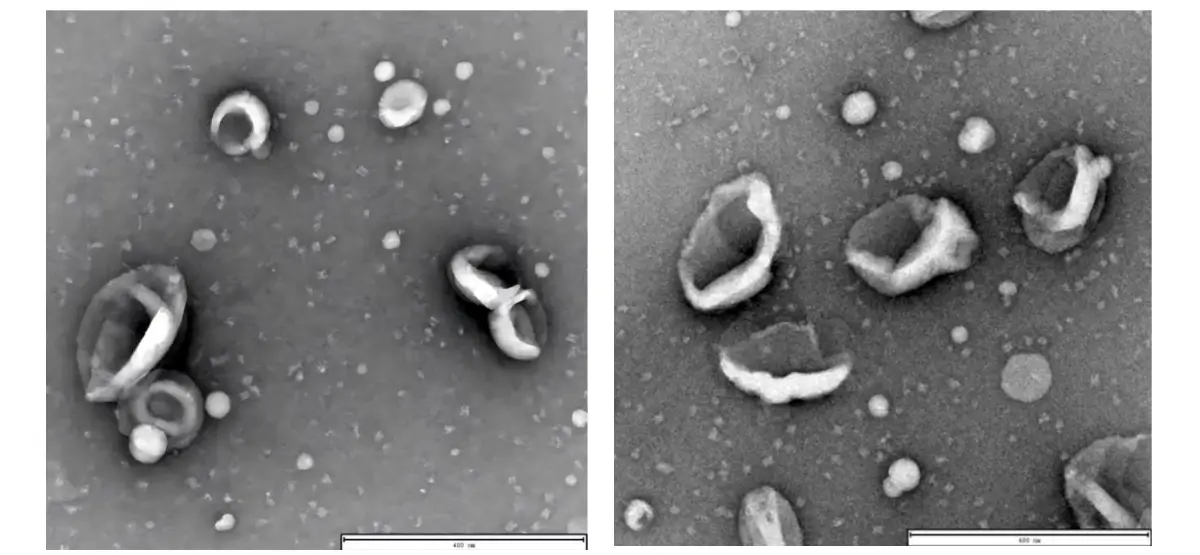
Caracterização morfológica por microscopia eletrônica de transmissão (TEM)
A análise por TEM revelou morfologia característica em forma de taça e semelhante a uma placa, padrão consistente com a literatura para exossomos de origem plasmática. A barra de escala de 400 nm confirma que as partículas estão na faixa esperada para small EVs.
A preservação da morfologia após o processo indica ausência de desnaturação proteica ou ruptura de membrana, condição necessária para que análises funcionais subsequentes produzam dados válidos.
Rendimento e pureza: EXODUS H-600 vs. ultracentrifugação vs. PEG
Comparação direta entre os três métodos a partir de 20 µL de plasma (≈ 2 × 10¹⁰ partículas/mL), conforme documentado pela Exodus Bio:
- Rendimento: EVs isoladas pelo EXODUS H-600 e por PEG apresentaram aumento de mais de 50 vezes em relação à UC.
- Pureza: a pureza das sEVs pelo EXODUS H-600 foi mais de três vezes superior à obtida por UC ou PEG.
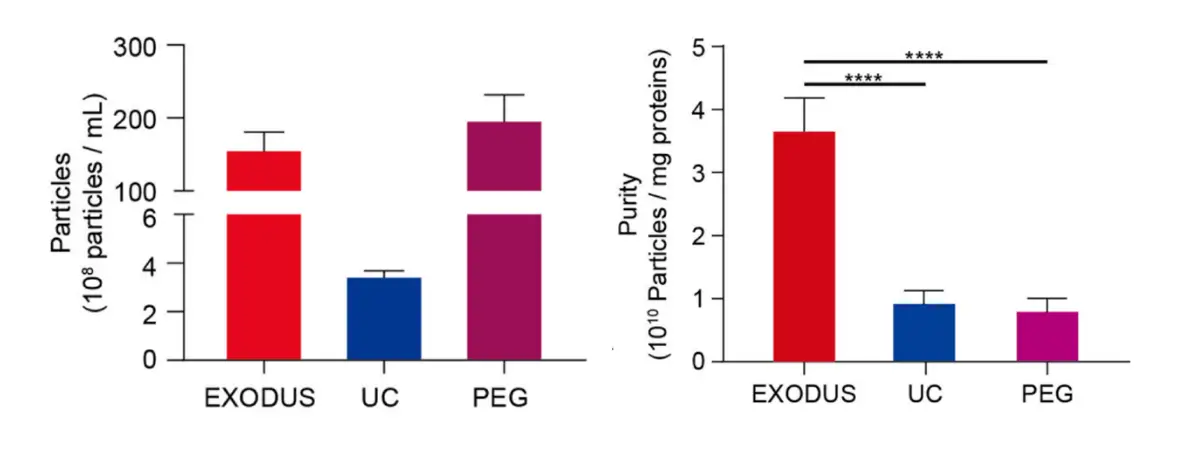
A combinação de alto rendimento com alta pureza é o diferencial crítico do EXODUS H-600. Enquanto o PEG apresenta rendimento comparável, sua pureza é significativamente inferior, comprometendo análises downstream sensíveis como proteômica e transcriptômica.
Isolamento de EVs Plasmáticas com o EXODUS T-2800: Resultados Experimentais
O T-2800 foi caracterizado por três abordagens complementares, cobrindo morfologia, identidade molecular e perfil de tamanho e concentração.

Caracterização morfológica por TEM
A microscopia eletrônica revelou as formas características em taça e placa dos exossomos isolados com o T-2800, barra de escala de 400 nm. A morfologia preservada confirma que o mecanismo de baixo cisalhamento opera de forma equivalente no modelo compacto.
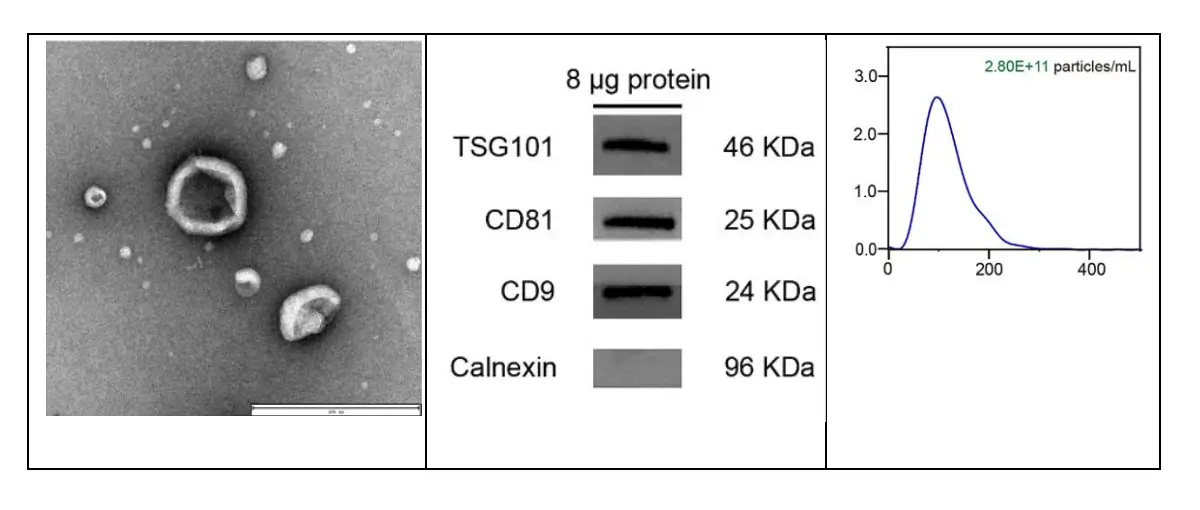
Confirmação de marcadores por Western Blot
A identidade dos exossomos foi validada por Western blot com painel de marcadores canônicos:
- Positivos (detectados): TSG101, CD81 e CD9 — proteínas de membrana e endossomais, marcadores padrão de exossomos segundo as diretrizes da ISEV.
- Negativo (não detectado): calnexina — proteína residente do retículo endoplasmático, cuja ausência confirma ausência de contaminação por debris de organelas.
A detecção de marcadores positivos combinada à ausência de calnexina é o critério padrão para validação de pureza de exossomos segundo as recomendações internacionais da ISEV (MISEV2018).
Análise por NTA: tamanho e concentração das partículas isoladas
A análise por rastreamento de nanopartículas (NTA) demonstrou tamanho médio de 100 nm e concentração de 2,8 × 10¹¹ partículas/mL, valores consistentes com o perfil esperado para small EVs de origem plasmática e adequados para experimentos downstream.
H-600 vs. T-2800: quando usar cada modelo
Ambos compartilham o mesmo princípio de nanofiltração com NPO e HO, mas diferem em escala e perfil de aplicação:
- EXODUS H-600: modelo compacto de bancada, ideal para pesquisa e múltiplas amostras em laboratório. Processa de 10 µL a 250 mL, até 200 mL/h.
- EXODUS T-2800: sistema de grande escala para manufatura GMP, indicado para volumes maiores e produção em larga escala.
Para aplicações clínicas ou translacionais com plasma em larga escala, o H-600 oferece maior capacidade. Para caracterização de amostras específicas ou validação de protocolo, o T-2800 é alternativa prática e eficiente.
Aplicações do isolamento de EVs plasmáticas em pesquisa biomédica
O plasma é uma das matrizes mais utilizadas em pesquisa com EVs por ser acessível, minimamente invasivo e rico em vesículas de origem sistêmica. A qualidade do isolamento determina diretamente a validade das análises realizadas.
- Biomarcadores em oncologia: exossomos plasmáticos carregam proteínas, miRNAs e DNA tumoral exploráveis como biomarcadores de diagnóstico e monitoramento terapêutico.
- Biópsia líquida: viabiliza análises não invasivas com potencial para complementar biópsias teciduais em contextos clínicos.
- Doenças inflamatórias e metabólicas: EVs plasmáticas têm sido investigadas em condições como sepse, diabetes e doenças cardiovasculares.
- Terapias baseadas em EVs: o isolamento de alta pureza é pré-requisito para desenvolvimento de EVs como veículos terapêuticos.
A qualidade do isolamento não é uma etapa técnica secundária, ela define o que pode ou não ser concluído a partir dos dados gerados. Métodos com baixa pureza introduzem ruído molecular que compromete qualquer análise downstream.
Perguntas Frequentes sobre o EXODUS e o Isolamento de EVs em Plasma
O EXODUS pode processar plasma diretamente, sem pré-tratamento?
Sim, conforme documentado pela Exodus Bio. Os experimentos utilizaram plasma como matriz direta, sem etapas de pré-clarificação extensas.
Qual o volume mínimo de plasma necessário para isolamento com o H-600?
O H-600 processa volumes a partir de 10 µL, compatível com amostras clínicas de volume limitado.
Por que a pureza do EXODUS é superior à do PEG, se o rendimento é similar?
O PEG precipita indiscriminadamente proteínas e macromoléculas junto com as EVs. O EXODUS retém as partículas por tamanho via membrana nanoporosa, removendo seletivamente impurezas menores.
Os marcadores TSG101, CD81 e CD9 são suficientes para validar exossomos?
São os marcadores recomendados pelas diretrizes MISEV2018 da ISEV para caracterização mínima de exossomos, junto à ausência de marcadores negativos como calnexina.
O que é NTA e por que é usado na caracterização de EVs?
NTA (Nanoparticle Tracking Analysis) rastreia o movimento browniano de partículas para determinar distribuição de tamanho e concentração. É o método padrão para caracterização quantitativa de EVs.
O EXODUS T-2800 produz resultados equivalentes ao H-600?
Os dados de TEM, Western blot e NTA do T-2800 são consistentes com os padrões de qualidade do H-600. Ambos utilizam o mesmo mecanismo central de isolamento.
O EXODUS H-600 e o T-2800 estão disponíveis no Brasil?
Sim. Ambos os modelos são distribuídos no Brasil pela Dafratec, distribuidora especializada em equipamentos científicos de alta precisão.