Um biorreator é um equipamento especializado que fornece ambiente controlado para o crescimento de microrganismos, células ou enzimas em processos biotecnológicos. Este sistema mantém condições ideais de temperatura, pH, oxigênio dissolvido e agitação, permitindo cultivos celulares e fermentações com alta eficiência e reprodutibilidade. Segundo dados da National Center for Biotechnology Information, o mercado global de biorreatores deve crescer 8,2% anualmente até 2028, impulsionado pelo avanço da biotecnologia farmacêutica.
Este artigo abordará os principais aspectos dos biorreatores:
- Tipos de biorreatores e suas aplicações específicas
- Tecnologias de controle e monitoramento
- Vantagens operacionais de cada modelo
- Critérios para seleção do biorreator ideal
- Tendências futuras em bioprocessamento
- Aplicações industriais e de pesquisa
Tipos de Biorreatores Disponíveis no Mercado
O mercado oferece diversos tipos de biorreatores, desde microbiorreatores para screening até sistemas de produção industrial. Cada modelo apresenta características específicas que atendem diferentes necessidades de pesquisa e produção. Os biorreatores variam em capacidade, tecnologia de controle, materiais de construção e aplicações específicas em biotecnologia moderna.
A escolha do biorreator adequado depende de fatores como tipo de cultivo celular, volume de produção de bioinsumos, requisitos de esterilização e nível de automação desejado. Sistemas modernos integram tecnologias avançadas de sensoriamento para preservação de bioamostras e controle automatizado.
Microbiorreator BioLector: Inovação em Alto Rendimentos
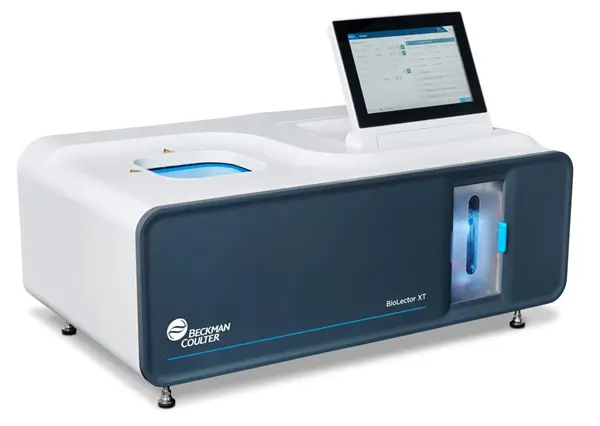
O biorreator BioLector representa uma revolução no bioprocessamento de alto rendimento. Este microbiorreator BioLector utiliza tecnologia de placa de microtitulação com 48 poços, permitindo avaliação simultânea de múltiplas condições.
Características principais do biorreator BioLector incluem sensores ópticos pré-calibrados para medição de biomassa, fluorescência, pH e densidade óptica em tempo real. O módulo microfluídico opcional elimina tubulações complexas, oferecendo operação simplificada para cultivo celular.
Biorreator de Bancada KLF: Único Sistema Esterilizável In Situ
O biorreator de bancada KLF da Bioengineering é o único fermentador de vidro esterilizável in situ disponível mundialmente. Esta exclusividade tecnológica representa avanço decisivo em bioprocessos laboratoriais.
Disponível em capacidades de 1,6L a 3,7L, este biorreator utiliza vaso de vidro borossilicato com sistema de agitação inferior. A esterilização in situ com meio agitado elimina riscos de contaminação durante transferências, oferecendo processo comparável a fermentadores industriais.
O sistema inclui software BioSCADA integrado e suporte para até 6 biorreatores por unidade de controle. A transparência total do vidro permite monitoramento visual direto sem interromper o processo estéril, fundamental para preservação de bioamostras em cultivo celular.
Biorreator NLF: Solução Avançada para Produção Piloto
O biorreator NLF da Bioengineering atende necessidades de produção piloto com capacidades de 11 a 20 litros. Este sistema móvel e modular oferece solução eficiente para empresas que buscam escalabilidade.
Desenvolvido em conformidade com normas FDA e GMP, o biorreator NLF inclui documentação completa para aplicações pré-clínicas. Sistemas de automação avançada reduzem erro humano e aumentam precisão nos processos.
O design adaptado facilita estudos de escalabilidade, garantindo que resultados obtidos sejam replicáveis em larga escala. Ideal para testes de escala-up e desenvolvimento de bioprodutos farmacêuticos.
Biorreator Modular RALF: Design Compacto e Eficiente
O biorreator RALF combina design compacto com funcionalidade avançada. Este equipamento versátil ocupa espaço mínimo no laboratório, mantendo todas as funcionalidades de sistemas maiores.
Características exclusivas incluem condensador de refluxo dobrável, alças retráteis para autoclavagem e configuração modular flexível. O sistema permite troca entre cultivo microbiano e celular no mesmo equipamento.
Três opções de controle de temperatura estão disponíveis: defletores ocupados, recipiente de dupla camisa e almofada de aquecimento. O software BioSCADA RALF oferece automação completa com interface intuitiva.
Série LP e P: Biorreatores de Alta Capacidade
Os biorreatores LP e P são baseados na plataforma NLF, oferecendo maior capacidade para produção. Disponíveis de 28 a 650 litros, atendem desde estudos de escalonamento até produção clínica.
Adequados para produção de bactérias, leveduras, células animais e vegetais, estes biorreatores incluem documentação GMP completa. Opções especializadas incluem filtro rotativo para perfusão e gaseificação sem bolhas.
A instalação é rápida e simples, com conexões centrais que minimizam tempo de setup. Sistema de correia reduz altura do tanque, facilitando acesso para todas as operações.
Planta de Biofermentadores: Soluções Industriais
A planta de biofermentadores da Bioengineering oferece sistemas personalizados de 30 a 50.000 litros. Cada sistema é otimizado para culturas específicas com geometria típica h:d = 3:1.
Tecnologias avançadas garantem alto coeficiente de transferência de massa (kLa) e suprimento ideal de oxigênio. Soluções integradas incluem tanques de dosagem para ácidos e antiespumantes.
Com mais de 50 anos de experiência, a Bioengineering oferece suporte técnico especializado para fermentação contínua e processos com alta demanda de oxigênio. Sistemas adaptados atendem requisitos específicos de biossegurança e formação de espuma.
Biorreatores de Produção: 30 a 25.000 Litros
Os biorreatores de produção da Bioengineering atendem cultura de células de mamíferos, vegetais, insetos e vírus. Capacidades variam de 30 a 25.000 litros para diferentes escalas produtivas.
Design especializado acomoda células em suspensão e aderentes com estratégias de aeração, gaseificação e perfusão adaptadas. Sistemas de esterilização são otimizados para meios termo-sensíveis.
A integração com integradores e fornecimento de tanques auxiliares aceleram implementação. Redução significativa do tempo operacional aumenta produtividade geral dos processos de cultura celular.
Mercado de Bioinsumos e Biocombustíveis: Crescimento Exponencial
O mercado brasileiro de bioinsumos experimenta crescimento acelerado, movimentando R$ 5 bilhões na safra 2023/2024, com taxa de crescimento de 15% anual segundo a CropLife Brasil. O setor apresenta taxa média anual de crescimento de 21% nos últimos três anos, quatro vezes acima da média global.
Os bioinsumos incluem produtos de controle biológico, inoculantes, bioestimulantes e solubilizadores, produzidos através de cultivo celular especializado em biorreatores. Segundo dados da Embrapa, o mercado brasileiro atingiu R$ 1 bilhão em 2020-2021, com projeção de R$ 17 bilhões até 2030.
Setor de Biocombustíveis em Expansão
O Brasil atingiu produção recorde de biocombustíveis em 2024, com 36,83 bilhões de litros de etanol segundo a UNICA. A produção de etanol a partir do milho cresceu 32,8%, totalizando 7,7 bilhões de litros, demonstrando diversificação das matérias-primas para biocombustíveis.
Dados da ANP mostram que a produção conjunta de etanol e biodiesel alcançou quase 43 bilhões de litros em 2023. O biometano apresentou crescimento de 12,3%, atingindo 74,9 milhões de m³, evidenciando a expansão da biotecnologia para diferentes tipos de biocombustíveis.
Aplicações em Biotecnologia Avançada
Os biorreatores desempenham papel fundamental na produção de bioamostras para pesquisa em biotecnologia, incluindo desenvolvimento de vacinas, medicamentos biotecnológicos e produtos para criogenia. O cultivo celular controlado permite produção de células especializadas para terapias avançadas e medicina regenerativa.
A biotecnologia farmacêutica utiliza biorreatores para produção de proteínas terapêuticas, anticorpos monoclonais e outros produtos biológicos. Sistemas de preservação através de criogenia dependem de bioamostras produzidas em condições controladas de cultivo celular.
Vantagens dos Biorreatores Modernos
Biorreatores modernos oferecem vantagens significativas sobre métodos tradicionais de cultivo celular. O controle preciso de parâmetros críticos resulta em maior produtividade e reprodutibilidade dos processos biotecnológicos, essenciais para produção de bioinsumos e biocombustíveis.
Sistemas automatizados reduzem intervenção manual, minimizando riscos de contaminação de bioamostras. Sensores avançados permitem monitoramento em tempo real de biomassa, pH, oxigênio dissolvido e outros parâmetros essenciais para cultivo celular otimizado.
Tecnologias de Controle Avançado
Tecnologias modernas de controle incluem sensores ópticos, medição gravimétrica e análise de gases de exaustão. Estes sistemas oferecem precisão superior e resposta rápida a variações no processo de cultivo celular, fundamentais para produção confiável de bioinsumos.
Software especializado permite programação de receitas, controle de cascatas e geração automática de relatórios para biotecnologia farmacêutica. Interfaces intuitivas facilitam operação sem necessidade de conhecimento em programação, democratizando o acesso às tecnologias de criogenia e preservação.
Aplicações Industriais Específicas
Biorreatores atendem diversas aplicações industriais, desde produção farmacêutica até biotecnologia alimentícia com foco em bioinsumos. Cada setor apresenta requisitos específicos de design, controle e documentação para cultivo celular especializado.
Na indústria farmacêutica, biorreatores devem atender normas GMP rigorosas para produção de bioamostras. Aplicações em pesquisa de biocombustíveis requerem flexibilidade para diferentes tipos de experimentos e condições de cultivo otimizadas.

Seleção do Biorreator Ideal
A seleção do biorreator adequado depende de múltiplos fatores técnicos e operacionais para aplicações em biotecnologia. Volume de produção de bioinsumos, tipo de cultivo celular, requisitos de esterilização e nível de automação são considerações fundamentais.
Biorreatores de bancada são ideais para pesquisa e desenvolvimento de biocombustíveis, oferecendo flexibilidade e facilidade operacional. Sistemas de produção requerem maior capacidade e conformidade regulatória para biotecnologia industrial.
Critérios de Avaliação
Critérios importantes incluem capacidade de processamento, materiais de construção para cultivo celular, sistemas de controle para bioamostras e suporte técnico disponível. Custo operacional e facilidade de manutenção também influenciam a decisão para produção de bioinsumos.
Tendências Futuras em Biorreatores
O desenvolvimento de biorreatores segue tendências de digitalização e automação avançada para biotecnologia moderna. Inteligência artificial e machine learning são integrados para otimização automática de processos de cultivo celular e produção de biocombustíveis.
Miniaturização de tecnologias permite desenvolvimento de microbiorreatores mais sofisticados para screening de bioinsumos. Sensores wireless e Internet das Coisas (IoT) revolucionam monitoramento remoto de bioprocessos e preservação de bioamostras.
FAQ - Perguntas Frequentes sobre Biorreatores
1. O que é um biorreator e como funciona?
Biorreator é equipamento que mantém condições controladas para crescimento de microrganismos ou células. Funciona regulando temperatura, pH, oxigênio dissolvido, agitação e outros parâmetros críticos para otimizar processos biotecnológicos.
2. Qual a diferença entre biorreator e fermentador?
Termos frequentemente usados de forma intercambiável, porém fermentador tradicionalmente refere-se a processos anaeróbios, enquanto biorreator é termo mais abrangente que inclui cultivos aeróbios e anaeróbios.
3. Quais tipos de biorreatores existem no mercado?
Principais tipos incluem microbiorreatores para screening, biorreatores de bancada para pesquisa, sistemas piloto para escalonamento e biorreatores de produção para manufatura industrial.
4. Como escolher o biorreator ideal para minha aplicação?
Considere volume de produção necessário, tipo de cultivo, requisitos de esterilização, nível de automação desejado, orçamento disponível e suporte técnico oferecido pelo fabricante.
5. Qual a importância do controle de pH em biorreatores?
pH adequado é crucial para viabilidade celular e produtividade. Variações podem afetar metabolismo, crescimento e produção de metabólitos. Sistemas automatizados mantêm pH dentro de faixas ideais.
6. Biorreatores requerem manutenção especializada?
Sim, manutenção regular inclui calibração de sensores, verificação de vedações, limpeza de sistemas e validação de performance. Fabricantes oferecem treinamento e suporte técnico especializado.
7. É possível escalar processos de biorreatores de bancada para produção?
Sim, com planejamento adequado. Parâmetros como potência de agitação, transferência de massa e tempo de mistura devem ser mantidos proporcionais durante escalonamento.
Leituras Relacionadas
Para aprofundar conhecimento em bioprocessamento, sugerimos explorar os temas:
- Fermentação Industrial - Processos e tecnologias para produção em larga escala
- Cultivo Celular - Técnicas avançadas para cultura de células animais e vegetais
- Bioengenharia de Processos - Otimização e controle de bioprocessos industriais