Os polímeros celulósicos HPMC (hidroxipropilmetilcelulose), HPC (hidroxipropilcelulose) e HEC (hidroxietilcelulose) são excipientes hidrofílicos amplamente utilizados em formulações farmacêuticas de liberação modificada. Cada um apresenta propriedades físico-químicas distintas que determinam seu comportamento em contato com água e o perfil de liberação de fármacos. O HPMC é classificado como Generally Recognized as Safe (GRAS) pela FDA , reforçando sua segurança para uso farmacêutico global.
O mercado farmacêutico registra crescimento consistente na demanda por sistemas de liberação modificada. Pesquisas recentes, como o estudo de Baumgartner et al. publicado no European Journal of Pharmaceutical Sciences , demonstram que a caracterização detalhada de propriedades superficiais desses polímeros por técnicas como cromatografia gasosa inversa é essencial para prever seu desempenho em matrizes farmacêuticas e correlacionar dados superficiais com mecanismos de liberação.
- Diferenças estruturais entre HPMC, HPC e HEC e suas implicações
- Propriedades de polaridade, hidratação e intumescimento
- Dados experimentais de entalpia de adsorção e números ácido-base
- Mecanismos de liberação: difusão vs relaxação polimérica
- Influência do tamanho molecular do fármaco na cinética de liberação
- Técnicas analíticas: IGC e DVS para caracterização superficial
- Aplicações práticas e critérios de escolha entre os polímeros
O que são HPMC, HPC e HEC: Derivados de Celulose em Formulações Farmacêuticas
Os três polímeros derivam da celulose natural através de modificações químicas que introduzem grupos substituintes específicos. Essas substituições alteram radicalmente as propriedades de hidratação, solubilidade e capacidade de formação de gel do polímero original, conforme documentado em extensas revisões sobre matrizes hidrofílicas .
Cada polímero apresenta uma combinação única de propriedades que os torna adequados para diferentes aplicações farmacêuticas, desde liberação imediata modificada até sistemas de liberação sustentada prolongada.
HPMC: Hidroxipropilmetilcelulose e Suas Propriedades de Hidratação
O HPMC é um éter de celulose que contém grupos metil e hidroxipropil ligados à cadeia celulósica. Esta combinação de substituintes confere ao polímero características balanceadas entre hidrofilia e hidrofobia, resultando em propriedades de hidratação intermediárias e formação de gel controlada.
Segundo dados experimentais do estudo de Baumgartner et al., o HPMC Premium Methocel K4M possui peso molecular médio de aproximadamente 95.000 Da, com 22,9% de grupos metoxil e 9,2% de grupos hidroxipropoxil. Essa composição confere ao polímero uma viscosidade específica adequada para matrizes de liberação sustentada.
HPC: Hidroxipropilcelulose e Liberação por Difusão Fickiana
O HPC contém exclusivamente grupos hidroxipropil como substituintes, com substituição molar de aproximadamente 3,7 e peso molecular médio de 1.150.000 Da. A ausência de grupos metil torna o HPC menos hidrofílico que HPMC e HEC, resultando em menor capacidade de hidratação e intumescimento.
O HPC demonstra os menores valores de entalpia específica de adsorção entre os três polímeros estudados, indicando interações mais fracas com moléculas polares como água. Isso resulta em um mecanismo de liberação predominantemente difusional, regido pelas leis de Fick.
HEC: Hidroxietilcelulose e Mecanismo de Relaxação Polimérica
O HEC possui grupos hidroxietil com substituição molar de aproximadamente 2,5 e peso molecular médio de 1.200.000 Da. Os grupos etil são menores que os grupos propil do HPC, resultando em menor impedimento estérico e maior facilidade de hidratação.
O HEC demonstra a maior polaridade entre os três polímeros, com valores significativamente mais altos de entalpia específica de adsorção para todas as sondas polares testadas. Essa alta polaridade resulta em rápida hidratação, maior grau de intumescimento e forte contribuição do mecanismo de relaxação das cadeias poliméricas durante a liberação.
Comparação de Polaridade entre HPMC, HPC e HEC por Cromatografia Gasosa Inversa
A técnica de Cromatografia Gasosa Inversa (IGC) permite determinar com precisão as propriedades superficiais dos polímeros através da medição de interações com sondas moleculares conhecidas. No estudo referenciado, foram utilizadas sondas apolares (alcanos de hexano a decano) e polares (tetrahidrofurano, acetona, etilacetato e triclorometano).
A componente dispersiva da energia livre superficial (γˢᵈ) mostrou diferenças pequenas entre os polímeros, variando de 26 a 33 mN/m a 30°C. Porém, as propriedades polares revelaram diferenças significativas que explicam o comportamento distinto em meio aquoso.
A ordem de polaridade determinada por IGC foi consistente em todas as temperaturas testadas (30, 40, 50 e 60°C):
HEC > HPMC > HPC
Essa sequência correlaciona-se diretamente com a capacidade de hidratação e com o grau de intumescimento observado experimentalmente.
Entalpia de Adsorção e Números Ácido-Base: Dados Quantitativos de HPMC vs HPC vs HEC
A entalpia específica de adsorção (ΔH sp A ) quantifica as interações polares entre o polímero e moléculas de sonda. Valores mais negativos indicam interações exotérmicas mais fortes, refletindo maior afinidade por moléculas polares como a água.
Dados experimentais do estudo mostram diferenças marcantes entre os polímeros:
| Sonda Polar | HEC (kJ/mol) | HPMC (kJ/mol) | HPC (kJ/mol) |
|---|---|---|---|
| Acetona | -49 ± 4 | -30 ± 2 | -15 ± 2 |
| Tetrahidrofurano | -43 ± 4 | -22 ± 2 | -18 ± 2 |
| Etilacetato | -51 ± 4 | -41 ± 3 | -16 ± 1 |
| Triclorometano | -25 ± 2 | -9 ± 1 | -12 ± 1 |
A análise de propriedades ácido-base segundo o método de Gutmann (1978) revelou:
| Polímero | Ka (número ácido) | Kd (número base) |
|---|---|---|
| HEC | 0,474 | 1,658 |
| HPMC | 0,233 | 1,652 |
| HPC | 0,204 | 0,277 |
O HEC demonstra tanto maior acidez de Lewis (capacidade de aceitar elétrons) quanto maior basicidade (capacidade de doar elétrons) em comparação com HPMC e HPC. O HPMC apresenta basicidade similar ao HEC, mas com acidez intermediária. O HPC mostra os menores valores em ambos os parâmetros, confirmando sua menor polaridade geral.
Capacidade de Intumescimento de Matrizes de HPMC, HPC e HEC
O grau de intumescimento foi determinado experimentalmente através de medidas gravimétricas em água purificada a 37°C durante 8 horas. Os resultados demonstram diferenças significativas na capacidade de absorção de água entre os polímeros.
As matrizes de HEC apresentaram o maior grau de intumescimento, atingindo hidratação máxima em menor tempo. As matrizes de HPMC mostraram comportamento intermediário, enquanto as de HPC exibiram o menor grau de intumescimento ao longo de todo o período estudado.
Essa diferença no intumescimento tem impacto direto na espessura da camada de gel formada, na concentração de polímero no gel, no tamanho de poro da rede polimérica e, consequentemente, na velocidade de liberação do fármaco.
Figura 2 - Grau de intumescimento de comprimidos matriciais de éteres de celulose em função do tempo. Cada ponto representa a média de seis determinações.
Sorção Dinâmica de Vapor de Água em HPMC, HPC e HEC
A técnica de Sorção Dinâmica de Vapor (DVS) permitiu avaliar a higroscopicidade dos polímeros em pó sob diferentes condições de umidade relativa. Os três polímeros apresentaram isotermas de adsorção do tipo V segundo a classificação de Brunauer, características de materiais hidrofílicos.
A análise DVS confirmou que o HEC é o polímero mais higroscópico, seguido por HPMC e HPC. Essa sequência mantém-se constante em toda a faixa de umidade relativa testada (0-98%), validando os resultados obtidos por IGC e reforçando a correlação entre propriedades superficiais determinadas em condições secas e comportamento em ambiente aquoso.
Figura 1 - Variação da massa dos polímeros HEC, HPMC e HPC em equilíbrio sob diferentes atmosferas de umidade relativa empregando o método DVS (s: sorção; d: dessorção).
Liberação Controlada: Modelo de Peppas-Sahlin para HPMC, HPC e HEC
O modelo de Peppas-Sahlin permite separar matematicamente as contribuições dos mecanismos de difusão Fickiana e relaxação polimérica no processo global de liberação. Anteriormente, Ritger e Peppas propuseram uma equação baseada em lei de potência para descrever a cinética de liberação de sistemas controlados por intumescimento:
M t /M ∞ = k·t n (Equação 1)
Onde M t é a quantidade de fármaco liberada no tempo t, M ∞ é a quantidade liberada em tempo infinito, k é uma constante cinética e n é o expoente difusional que depende do mecanismo de liberação e da geometria do dispositivo.
Para melhor compreensão dos fenômenos envolvidos, Peppas e Sahlin (1989) desenvolveram um modelo que separa as contribuições difusionais e relaxacionais:
M t /M ∞ = k₁·t m + k₂·t 2m (Equação 9)
Onde:
- M t /M ∞ = fração de fármaco liberada no tempo t (até 60%)
- k₁ = constante cinética difusional
- k₂ = constante cinética relaxacional
- m = expoente difusional Fickiano (0,45 para geometria de placa)
Os dados experimentais para liberação de pentoxifilina (peso molecular 278,31 Da, volume molar 211,2 cm³/mol) e vancomicina (peso molecular 1485,73 Da, volume molar 874,6 cm³/mol) mostraram:
| Polímero | k₁ (%h⁻⁰·⁴⁵) | k₂ (%h⁻⁰·⁹⁰) | R² |
|---|---|---|---|
| Pentoxifilina | |||
| HEC | 11,213 | 8,575 | 0,9997 |
| HPMC | 14,622 | 4,709 | 0,9985 |
| HPC | 18,798 | 1,207 | 0,9975 |
| Vancomicina | |||
| HEC | 7,771 | 6,194 | 0,9932 |
| HPMC | 11,026 | 4,108 | 0,9990 |
| HPC | 14,844 | 1,863 | 0,9991 |
Expoente Difusional (n) e Mecanismo de Transporte em HPMC, HPC e HEC
O expoente difusional (n) da equação de Ritger e Peppas classifica o mecanismo de transporte do fármaco através da matriz polimérica hidratada. Para geometria de placa (comprimidos planos), a interpretação segundo Ritger e Peppas (1987) é:
- n = 0,5: Transporte Fickiano (difusão pura)
- 0,5 < n < 1,0: Transporte anômalo (difusão + relaxação)
- n = 1,0: Caso II (relaxação pura)
Os valores experimentais de n obtidos foram:
| Polímero | n (Pentoxifilina) | n (Vancomicina) | Mecanismo |
|---|---|---|---|
| HEC | 0,675 | 0,775 | Anômalo (forte relaxação) |
| HPMC | 0,619 | 0,613 | Anômalo (moderado) |
| HPC | 0,509 | 0,525 | Quase Fickiano |
Todos os valores situam-se na região de transporte anômalo, indicando que tanto difusão quanto relaxação contribuem para a liberação. Porém, nota-se que:
Influência do Tamanho Molecular do Fármaco na Liberação de HPMC, HPC e HEC
A comparação entre pentoxifilina (volume molar 211,2 cm³/mol) e vancomicina (volume molar 874,6 cm³/mol) revela que o tamanho molecular do fármaco influencia significativamente o mecanismo de liberação em sistemas controlados por intumescimento.
Para todos os polímeros, os valores de n foram maiores para vancomicina do que para pentoxifilina, indicando maior contribuição da relaxação polimérica na liberação de moléculas maiores. Isso ocorre porque:
- Moléculas pequenas difundem facilmente através dos poros iniciais da matriz
- Moléculas grandes requerem maior tamanho de poro, que só se forma após relaxação das cadeias
- O tempo necessário para relaxação adequada retarda a liberação inicial de fármacos grandes
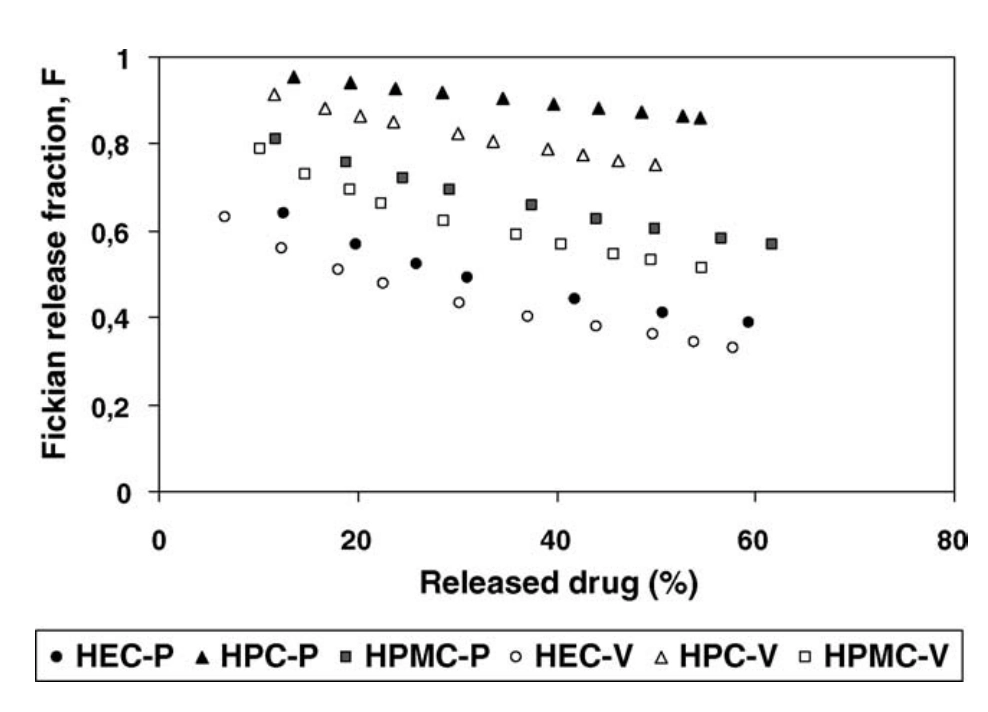
Figura 4 - Fração de liberação Fickiana F (Equação 10) em função da pentoxifilina (P) e vancomicina (V) liberadas de diferentes comprimidos de éteres de celulose. Desvio padrão < 2%.
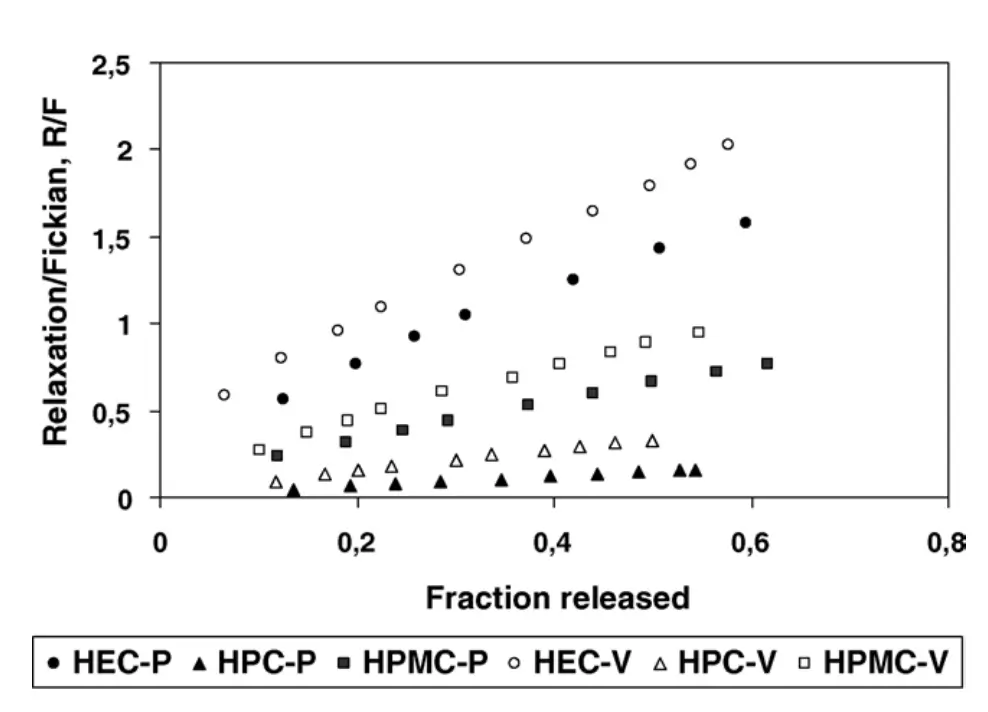
Figura 5 - Razão entre as contribuições relaxacional (R) e difusional (F) na liberação de pentoxifilina (P) e vancomicina (V) de diferentes comprimidos de éteres de celulose. Desvio padrão < 2%.
A taxa de liberação de ambos os fármacos seguiu consistentemente a ordem: HEC > HPMC > HPC, refletindo as diferenças de polaridade, hidratação e capacidade de relaxação dos polímeros.
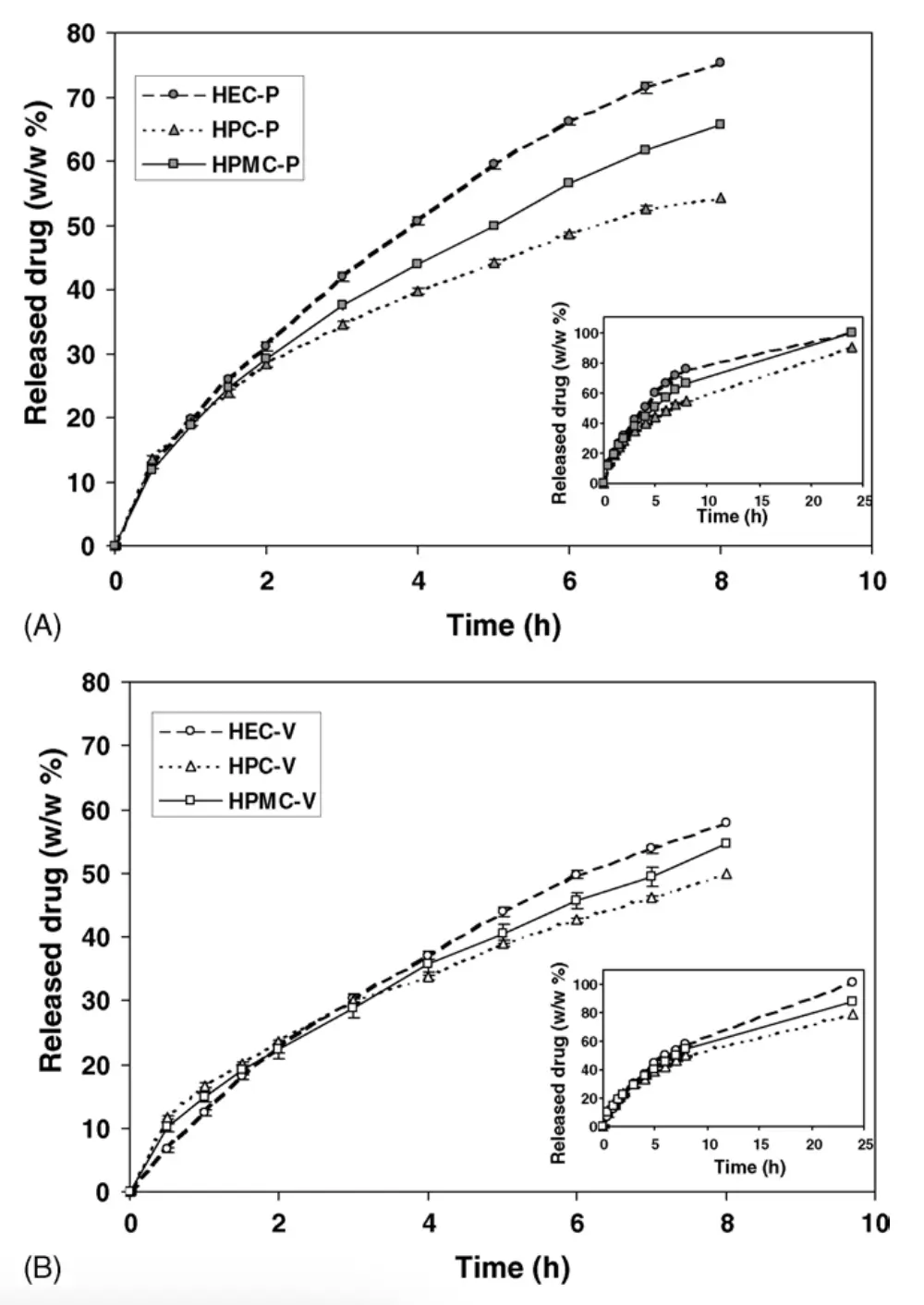
Figura 3 - Perfis de liberação de pentoxifilina (P) e cloridrato de vancomicina (V) de comprimidos baseados em diferentes polímeros éteres de celulose. Desvio padrão < 2%.
IGC (Inverse Gas Chromatography) para Caracterização Superficial de HPMC
A Cromatografia Gasosa Inversa é uma técnica termodinâmica que permite determinar propriedades superficiais de materiais particulados sem modificá-los quimicamente ou estruturalmente. Na IGC, o polímero em pó é a fase estacionária e moléculas de sonda com propriedades conhecidas são injetadas como fase móvel. A técnica tem sido amplamente utilizada para caracterização de excipientes farmacêuticos .
A técnica permite determinar:
- Energia livre superficial dispersiva (γ d s ): usando alcanos como sondas
- Entalpia específica de adsorção (ΔH sp A ): usando sondas polares
- Números ácido-base: através do método de Gutmann
- Temperatura de transição vítrea (Tg): em condições controladas
Para HPMC, a IGC revelou energia superficial dispersiva de 33,8 ± 2,5 mN/m a 30°C, diminuindo para 22,1 ± 2,1 mN/m a 60°C. Essa diminuição com a temperatura é esperada, pois interações intermoleculares enfraquecem em temperaturas mais altas.
IGC-SEA: Analisador Avançado de Energia de Superfície para Caracterização de Polímeros
O IGC-SEA (Surface Energy Analyzer) é um equipamento de cromatografia gasosa inversa de última geração projetado especificamente para caracterização superficial de materiais farmacêuticos, polímeros e excipientes. Este instrumento permite determinar com precisão as propriedades termodinâmicas superficiais que controlam interações entre materiais e seu ambiente.
Desenvolvido para atender aos mais rigorosos padrões de pesquisa e controle de qualidade farmacêutico, o IGC-SEA oferece automação completa e precisão excepcional na determinação de parâmetros críticos como energia superficial, polaridade, números ácido-base e propriedades de adsorção. A técnica é não destrutiva, requer quantidades mínimas de amostra e fornece dados quantitativos reprodutíveis essenciais para o desenvolvimento e otimização de formulações.

Principais benefícios do IGC-SEA:
- Caracterização completa: Determina energia superficial dispersiva, componentes polares, números ácido-base e entalpia de adsorção em uma única análise
- Alta reprodutibilidade: Sistema automatizado com controle preciso de temperatura e fluxo garante resultados consistentes entre lotes
- Análise rápida: Caracterização completa de um polímero em 4-6 horas, comparado a dias necessários para métodos tradicionais
- Quantidade mínima de amostra: Requer apenas 0,5-1,0 g de material, ideal para fases iniciais de desenvolvimento
- Método não destrutivo: A amostra pode ser recuperada após análise para outros testes
- Previsão de comportamento: Correlação direta entre parâmetros IGC e desempenho em formulação, como demonstrado neste estudo
- Controle de qualidade: Detecção de variações lote-a-lote em propriedades superficiais que afetam desempenho
- Conformidade regulatória: Dados quantitativos robustos para documentação de CMC (Chemistry, Manufacturing and Controls)
Interesse em Caracterização Superficial de Polímeros?
Descubra como o IGC-SEA pode otimizar o desenvolvimento das suas formulações de liberação controlada.
Saiba Mais Sobre o IGC-SEADVS (Dynamic Vapor Sorption) e Higroscopicidade de Polímeros Celulósicos
A Sorção Dinâmica de Vapor é uma técnica gravimétrica automatizada que mede a variação de massa de uma amostra em função da umidade relativa do ambiente. Um fluxo de gás inerte com umidade controlada passa sobre a amostra, e uma microbalança registra continuamente a massa. Esta técnica é amplamente utilizada para estudos de sorção em excipientes farmacêuticos .
A técnica DVS permite:
- Determinar isotermas de sorção e dessorção
- Quantificar higroscopicidade de excipientes
- Avaliar estabilidade em diferentes condições de armazenamento
- Identificar transições de fase induzidas por umidade
- Estudar cinética de sorção/dessorção
No estudo referenciado, os três polímeros apresentaram isotermas tipo V, indicando que a primeira camada de moléculas de água adsorvidas facilita a adsorção subsequente de mais água. Esse comportamento é típico de polímeros hidrofílicos com múltiplos sítios de ligação de hidrogênio.
A ordem de higroscopicidade determinada por DVS (HEC > HPMC > HPC) correlaciona-se perfeitamente com os parâmetros de polaridade obtidos por IGC, validando ambas as técnicas como métodos complementares de caracterização.
Correlação entre Propriedades Superficiais e Cinética de Liberação
A análise integrada dos dados demonstra correlação direta entre as propriedades superficiais dos polímeros (determinadas por IGC e DVS) e seu comportamento em sistemas de liberação controlada:
| Propriedade | HEC | HPMC | HPC |
|---|---|---|---|
| Polaridade (ΔH sp A ) | Maior | Intermediária | Menor |
| Higroscopicidade (DVS) | Maior | Intermediária | Menor |
| Grau de intumescimento | Maior | Intermediário | Menor |
| k₂ (constante relaxacional) | Maior | Intermediária | Menor |
| Velocidade de liberação | Mais rápida | Intermediária | Mais lenta |
| Mecanismo dominante | Relaxação | Difusão + Relaxação | Difusão |
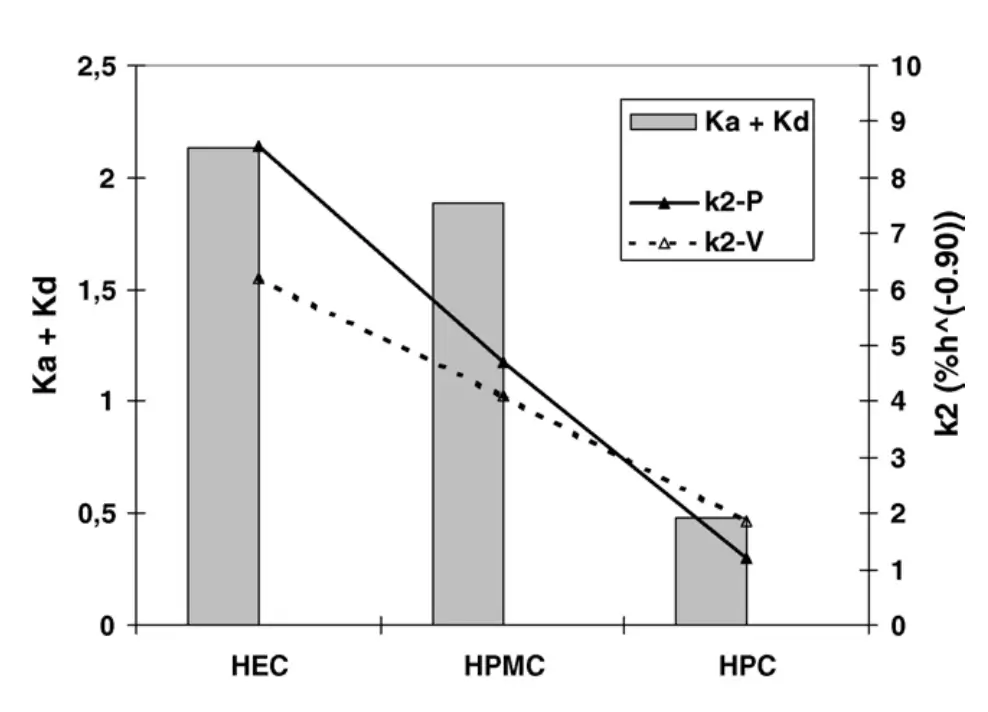
Figura 6 - Correlações entre a soma dos números ácido (Ka) e base (Kd) dos polímeros éteres de celulose e as constantes cinéticas relaxacionais k₂ para liberação de pentoxifilina e vancomicina desses comprimidos poliméricos.
Aplicações Práticas do HPMC em Formulações de Liberação Modificada
O HPMC é o polímero celulósico mais utilizado comercialmente em sistemas de liberação controlada devido ao seu perfil balanceado de propriedades. Suas principais aplicações incluem:
Comprimidos matriciais de liberação sustentada: O HPMC forma gel rapidamente ao contato com fluidos gastrointestinais, criando uma barreira que controla a liberação por 8-24 horas. Produtos comerciais como Metoprolol, Diltiazem e Teofilina de liberação prolongada utilizam matrizes de HPMC.
Revestimentos funcionais: Filmes de HPMC aplicados por spray-coating criam camadas de liberação entérica ou gastrorresistente. A permeabilidade do filme pode ser ajustada pela viscosidade do HPMC e adição de plastificantes.
Sistemas gastrorretentivos: Matrizes de HPMC de baixa densidade expandem no estômago, aumentando o tempo de residência gástrica e melhorando a biodisponibilidade de fármacos absorvidos na janela gástrica ou duodenal.
Cápsulas de liberação modificada: HPMC de baixa viscosidade pode ser incorporado em cápsulas de gelatina dura para modificar a liberação do conteúdo. Alternativamente, cápsulas feitas inteiramente de HPMC substituem gelatina em formulações vegetarianas.
Suspensões e emulsões: HPMC atua como agente espessante, estabilizante e formador de filme em formulações líquidas e semissólidas, controlando viscosidade e prevenindo sedimentação.
Quando Escolher HPC ou HEC em vez de HPMC
Apesar da versatilidade do HPMC, situações específicas podem favorecer o uso de HPC ou HEC:
Escolha HPC quando:
- For necessária liberação modificada com mínimo intumescimento
- O mecanismo difusional puro for adequado ao perfil desejado
- Houver restrições de espaço que limitem expansão do comprimido
- For necessária maior resistência mecânica inicial da matriz
- O fármaco for pequeno e hidrofílico (favorecendo difusão)
Escolha HEC quando:
- For desejada liberação rápida inicial seguida de liberação sustentada
- O fármaco for grande ou pouco solúvel (requerendo relaxação para liberação)
- For necessário alto grau de hidratação e formação rápida de gel
- Houver necessidade de bioadesão mucoadesiva significativa
- A formulação visar liberação em meio com baixa quantidade de água
Variabilidade Lote-a-Lote e Importância da Caracterização de HPMC
A reprodutibilidade de desempenho de matrizes de HPMC depende criticamente da consistência das propriedades do polímero entre diferentes lotes. Fatores que podem variar incluem:
- Viscosidade: Variações no peso molecular afetam a viscosidade da solução e a cinética de hidratação
- Grau de substituição: Pequenas diferenças na proporção de grupos metoxil e hidroxipropoxil alteram polaridade e hidrofilia
- Distribuição de substituintes: A homogeneidade da distribuição ao longo da cadeia influencia propriedades de gel
- Umidade residual: Afeta propriedades de fluxo, compressibilidade e estabilidade química
Técnicas como IGC e DVS permitem caracterizar essas variações de forma rápida e reprodutível, estabelecendo especificações mais rigorosas que os testes farmacopeicos tradicionais de viscosidade e perda por secagem.
HPMC como Polímero de Escolha para Matrizes Hidrofílicas
A análise comparativa detalhada entre HPMC, HPC e HEC demonstra que o HPMC ocupa posição privilegiada como excipiente para liberação controlada. Suas propriedades intermediárias de polaridade, hidratação e mecanismo de liberação proporcionam versatilidade incomparável.
Os dados experimentais de caracterização superficial por IGC correlacionam-se perfeitamente com o comportamento em meio aquoso, validando essas técnicas como ferramentas preditivas do desempenho de formulações. A entalpia específica de adsorção, os números ácido-base e a higroscopicidade determinada por DVS permitem prever:
- Velocidade de hidratação da matriz
- Grau de intumescimento
- Contribuição relativa de difusão vs relaxação
- Perfil de liberação para fármacos de diferentes tamanhos moleculares
Perspectivas futuras incluem o uso de inteligência artificial para correlacionar parâmetros de IGC/DVS com perfis de dissolução, permitindo desenvolvimento racional e acelerado de novas formulações baseadas em polímeros celulósicos.
Perguntas Frequentes sobre HPMC, HPC e HEC
1. Qual a principal diferença entre HPMC e HPC?
O HPMC contém grupos metil e hidroxipropil, enquanto o HPC contém apenas grupos hidroxipropil. Isso torna o HPMC mais hidrofílico, com maior capacidade de hidratação e mecanismo de liberação mais influenciado pela relaxação polimérica. O HPC libera fármacos principalmente por difusão Fickiana.
2. Por que o HEC hidrata mais rápido que HPMC e HPC?
O HEC possui grupos hidroxietil menores que os grupos propil, resultando em menor impedimento estérico e maior polaridade superficial. Dados de IGC mostram que o HEC apresenta entalpia de adsorção até 3 vezes mais negativa, indicando interações muito mais fortes com água.
3. O HPMC é seguro para uso farmacêutico?
Sim, o HPMC é classificado como GRAS (Generally Recognized As Safe) pela FDA e está presente em farmacopeias de todos os países. É utilizado em milhares de produtos farmacêuticos comerciais há décadas, com excelente perfil de segurança.
4. Como o tamanho do fármaco afeta a liberação de matrizes de HPMC?
Fármacos pequenos (volume molar < 300 cm³/mol) liberam principalmente por difusão através dos poros da matriz. Fármacos grandes (> 500 cm³/mol) dependem mais da relaxação das cadeias poliméricas para criar poros maiores, resultando em liberação mais lenta inicialmente.
5. Qual técnica mede a polaridade do HPMC de forma mais precisa?
A Cromatografia Gasosa Inversa (IGC) é considerada o padrão-ouro para determinação de polaridade superficial de polímeros em pó. Ela fornece valores quantitativos de entalpia de adsorção e números ácido-base que se correlacionam diretamente com comportamento em água.
6. HPMC pode ser usado em revestimentos entéricos?
O HPMC não é naturalmente gastrorresistente, mas pode ser modificado com grupos carboxílicos (HPMCAS - acetato-succinato de HPMC ou HPMCP - ftalato de HPMC) para criar revestimentos entéricos que resistem ao pH ácido gástrico.
7. Qual polímero libera fármacos mais rapidamente?
O HEC libera fármacos mais rapidamente devido à sua alta polaridade, rápida hidratação e forte contribuição da relaxação polimérica. A ordem experimental é: HEC > HPMC > HPC.
8. Como interpretar o expoente difusional n?
Para comprimidos planos: n = 0,5 indica difusão pura (Fickiana); 0,5 < n < 1,0 indica transporte anômalo (difusão + relaxação); n = 1,0 indica relaxação pura (Case II). Valores mais próximos de 0,5 significam maior controle difusional; valores mais próximos de 1,0 indicam maior controle por relaxação.
Leituras Relacionadas
- Matrizes Hidrofílicas para Liberação Controlada de Fármacos
- Técnicas de Caracterização Superficial de Polímeros Farmacêuticos
- Modelagem Matemática de Liberação: Equações de Higuchi, Korsmeyer-Peppas e Peppas-Sahlin

.webp)