As vesículas extracelulares (EVs) são pequenas bolhas com uma camada dupla de gordura na superfície. Elas são produzidas naturalmente por quase todas as células do corpo, desde bactérias até células humanas.

As EVs deixaram de ser vistas como “lixo celular” para se tornarem um dos temas mais quentes da biologia celular, oncologia, imunologia e medicina regenerativa.
Essas pequenas partículas delimitadas por membrana lipídica atuam como verdadeiros “correios” entre as células, transportando proteínas, lipídios, RNA e até DNA. Elas participam de praticamente todos os processos fisiológicos e patológicos.
Neste artigo completo e atualizado, você vai entender:
- O que são EVs e como são classificadas
- Sua evolução histórica e os principais marcos
- Por que concentração e fluorescência são críticas
- As melhores técnicas de isolamento e caracterização
- Diretrizes MISEV2023 e boas práticas para estudos reprodutíveis
Vamos começar.
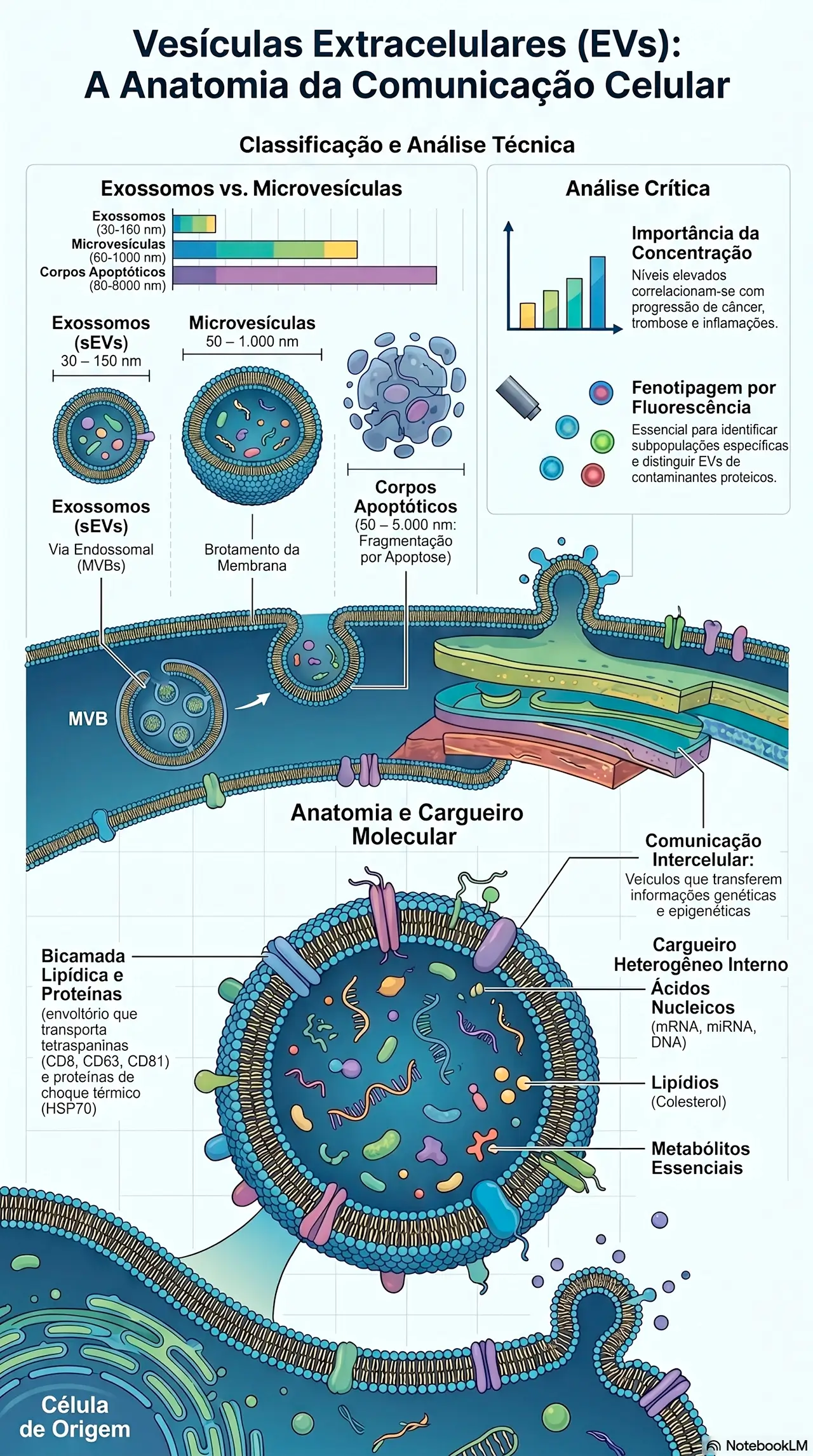
1. O que são Vesículas Extracelulares (EVs)?
As vesículas extracelulares (EVs) são partículas delimitadas por uma bicamada lipídica, liberadas naturalmente por praticamente todos os tipos de células, de bactérias a células humanas.
Elas não se replicam (não possuem núcleo funcional) e funcionam como veículos de comunicação intercelular, carregando um cargueiro molecular heterogêneo:
- Proteínas: tetraspaninas (CD9, CD63, CD81), proteínas de choque térmico (HSP70), Alix e TSG101
- Lipídios: colesterol, esfingomielina, ceramidas e fosfolipídios
- Ácidos nucleicos: mRNA, miRNA, lncRNA e DNA (mitocondrial ou genômico)
- Metabólitos e, ocasionalmente, fragmentos citoplasmáticos ou organelas
Características principais:
- Tamanho: variam de ~30 nm até >5 µm, mas a maioria fica abaixo de 200 nm
- Alta heterogeneidade: dependem da célula de origem, estado fisiológico/patológico e estímulos ambientais
- Composição dinâmica: muitas EVs apresentam uma “corona” de moléculas adsorvidas do ambiente extracelular
Classificação (atualizada pela MISEV2023)
A MISEV2023 (Welsh et al., 2024) recomenda evitar nomenclatura excessivamente rígida e priorizar a caracterização funcional. Ainda assim, as categorias mais usadas são:
- Pequenas EVs (sEVs / exossomos): 30–150 nm, originam-se da via endossomal (multivesicular bodies)
- EVs de tamanho médio (microvesículas ou ectossomos): 50–1.000 nm, formadas por brotamento direto da membrana plasmática
- Corpos apoptóticos: 50–5.000 nm, liberados durante apoptose
Importante: O termo genérico “EVs” é o mais seguro. A distinção exata entre subtipos ainda é desafiadora devido à sobreposição de propriedades e à presença de partículas não vesiculares (NVEPs), como lipoproteínas e agregados proteicos.
Funções principais:
- Comunicação paracrina e autócrina
- Transferência horizontal de informação genética e epigenética
- Modulação da resposta imune, angiogênese, coagulação e metabolismo
- Papel central em patologias: progressão tumoral, inflamação crônica, infecções e doenças neurodegenerativas
Em muitas doenças, a concentração de EVs circulantes no plasma aumenta significativamente.
2. História e Principais Estudos sobre EVs
A trajetória das EVs é um ótimo exemplo de como a ciência muda de paradigma.
- 1940–1980: Observadas inicialmente como “micropartículas plaquetárias” envolvidas na coagulação ou vesículas liberadas por reticulócitos.
- 1983–1987: Rose Johnstone e colaboradores descrevem os “exossomos” em reticulócitos, vesículas de 30–100 nm que não eram mero debris.
- 2007: Valadi et al. mostram que EVs carregam RNA funcional (mRNA e miRNA) e podem transferi-lo entre células, marco fundamental.
- 2010 em diante: Explosão de publicações. Reconhecimento do papel das EVs de células-tronco mesenquimais (MSCs) na regeneração e das EVs tumorais na metástase e imunossupressão.
Hoje, o campo cresce exponencialmente. As diretrizes MISEV (2014 → 2018 → 2023) foram fundamentais para padronizar o estudo das EVs.
A MISEV2023, publicada em fevereiro de 2024 no Journal of Extracellular Vesicles (Welsh et al.), contou com a contribuição de mais de mil pesquisadores e traz recomendações atualizadas desde abordagens básicas até avançadas (ômica integrada, estudos in vivo e reporting transparente).
3. Por que Concentração e Fluorescência são tão Importantes?
Devido à enorme heterogeneidade das EVs, dois parâmetros são essenciais para estudos rigorosos:
Concentração (partículas/mL)
- Reflete o estado celular: células tumorais ou estressadas liberam muito mais EVs.
- Valores típicos:
- Plasma de indivíduos saudáveis: ~1–2 × 10¹⁰ EVs/mL
- Pacientes com câncer (ex.: glioblastoma): pode chegar a 3–7 × 10¹⁰ EVs/mL ou mais (até 3–5 vezes maior)
- Em câncer de mama ou outros tumores sólidos: frequentemente 5–40 vezes maior que controles saudáveis
- Aplicações: dosagem reprodutível em terapia com EVs, comparação entre condições experimentais e uso como biomarcador em liquid biopsy.
Fluorescência
- Permite identificar subpopulações específicas (ex.: EVs CD63+, CD9+, EpCAM+ ou marcadores tumorais).
- Técnicas como fluorescence NTA (fl-NTA) e nano-flow cytometry (nanoFCM) permitem análise single-vesicle.
- Limite de detecção típico no nanoFCM: ~4–10 moléculas de anticorpo por partícula.
- Essencial para rastrear uptake celular, estudar destino intracelular e aumentar especificidade (distinguindo EVs de contaminantes).
A MISEV2023 enfatiza fortemente a necessidade de relatar concentração, distribuição de tamanho e marcadores fluorescentes para garantir reprodutibilidade.
4. Técnicas Usadas no Estudo de Vesículas Extracelulares
O fluxo de trabalho típico envolve: produção → isolamento → caracterização → aplicações funcionais.
a) Isolamento e Enriquecimento
Não existe método “puro”. A MISEV2023 recomenda combinar técnicas e sempre relatar recuperação e pureza.
Métodos mais usados:
- Ultracentrifugação diferencial (dUC): clássica, mas pode causar agregação
- Gradiente de densidade (iodixanol ou sacarose): melhora pureza
- Cromatografia de exclusão de tamanho (SEC): preserva melhor a integridade
- Imunoafinidade (beads magnéticos anti-CD9/CD63): alta especificidade para subpopulações
- Precipitação com polímeros (PEG): rápida, mas baixa pureza
Melhor prática atual: combinação de dUC + SEC ou imunoafinidade + SEC.
b) Caracterização Física
| Técnica | Faixa típica de tamanho | Vantagem principal | Limitação principal |
|---|---|---|---|
| Nanoparticle Tracking Analysis (NTA) | 50–1.000 nm | Distribuição de tamanho + concentração | Sensibilidade menor em partículas <50 nm |
| Nano-flow Cytometry (nanoFCM) | ~40–1.000 nm | Análise single-vesicle + fluorescência | Requer calibração rigorosa |
| Tunable Resistive Pulse Sensing (tRPS) | Variável | Medição precisa de tamanho/concentração | Menos usado que NTA/nanoFCM |
| Microscopia Eletrônica (cryo-TEM) | Todas | Confirmação da estrutura bicamada | Baixo throughput |
| Dynamic Light Scattering (DLS) | Média | Rápido | Pouca resolução em amostras polidispersas |
c) Caracterização Bioquímica
- Western Blot / ELISA: detecção de marcadores positivos (CD9, CD63, TSG101, Alix) e negativos (calnexina, histonas, APOA1/APOB).
- Omics integrados: proteômica (LC-MS/MS), transcriptômica (NGS) e lipidômica.
A MISEV2023 categoriza os marcadores em níveis de especificidade para facilitar a interpretação.
d) Ensaios Funcionais
- Testes de uptake (EVs marcadas com PKH, DiI ou proteínas fluorescentes)
- Ensaios de proliferação, migração, resposta imune e modulação tumoral
- Estudos in vivo de biodistribuição
Conclusão: O Futuro das Vesículas Extracelulares
As EVs representam uma revolução na forma como entendemos a comunicação celular. Elas já são estudadas como biomarcadores em liquid biopsy, veículos para terapia celular (especialmente EVs derivados de MSCs) e alvos em oncologia e doenças inflamatórias.
Com as diretrizes MISEV2023, o campo ganha muito mais rigor e reprodutibilidade. Quem dominar as técnicas de isolamento, quantificação precisa (NTA + nanoFCM) e caracterização funcional estará na vanguarda dessa área promissora.
FAQ – Vesículas Extracelulares (EVs)
1. O que são vesículas extracelulares (EVs) e qual é sua principal função?
As vesículas extracelulares (EVs) são pequenas partículas delimitadas por uma bicamada lipídica, liberadas por praticamente todos os tipos de células. Elas atuam como “correios” intercelulares, transportando proteínas (como CD9, CD63, CD81, Alix e TSG101), lipídios, RNA (mRNA, miRNA) e até DNA. Sua principal função é a comunicação paracrina e autócrina, além de modular processos como resposta imune, angiogênese e progressão de doenças.
2. Como as EVs são classificadas segundo as diretrizes MISEV2023?
A MISEV2023 recomenda evitar nomenclatura muito rígida e priorizar a caracterização funcional. As categorias mais usadas são:
- Pequenas EVs (sEVs / exossomos): 30–150 nm, originadas da via endossomal.
- EVs de tamanho médio (microvesículas): 50–1.000 nm, formadas por brotamento da membrana plasmática.
- Corpos apoptóticos: 50–5.000 nm, liberados durante apoptose. O termo genérico “EVs” é o mais recomendado devido à sobreposição entre subtipos.
3. Por que a concentração de EVs é importante nos estudos?
A concentração reflete o estado celular: células tumorais ou estressadas liberam muito mais EVs. Valores típicos:
- Plasma saudável: ~1–2 × 10¹⁰ EVs/mL
- Pacientes com câncer (ex.: glioblastoma): frequentemente 3–7 × 10¹⁰ EVs/mL ou até 5–40 vezes maior que controles saudáveis. Ela é essencial para dosagem reprodutível em terapias, comparação entre experimentos e uso como biomarcador em liquid biopsy.
4. Quais são as principais técnicas de caracterização física das EVs?
As técnicas mais utilizadas são:
- Nanoparticle Tracking Analysis (NTA): mede distribuição de tamanho e concentração (faixa típica 50–1.000 nm).
- Nano-flow Cytometry (nanoFCM): permite análise single-vesicle com fluorescência.
- Cryo-TEM: confirma a estrutura bicamada lipídica.
- SEC (Cromatografia de exclusão de tamanho) e imunoafinidade: usadas para isolamento com boa integridade ou especificidade. A MISEV2023 recomenda combinar métodos e relatar pureza e recuperação.
5. O que é a MISEV2023 e por que ela é importante?
A MISEV2023 (Welsh et al., 2024) é a atualização mais recente das diretrizes da International Society for Extracellular Vesicles (ISEV). Publicada no Journal of Extracellular Vesicles, contou com a contribuição de mais de mil pesquisadores. Ela padroniza produção, isolamento, caracterização e relatórios de estudos com EVs, desde abordagens básicas até avançadas (ômica integrada e estudos in vivo). Seu objetivo principal é aumentar a reprodutibilidade e o rigor científico no campo.