Vírus e VLPs como Ferramentas Científicas e Terapêuticas
Por serem patógenos em nanoescala com alta especificidade estrutural e capacidade de replicação, os vírus são amplamente utilizados em diversos campos, incluindo a biologia molecular, o desenvolvimento de vacinas e a terapia gênica. As partículas semelhantes a vírus (VLPs), estruturas ocas formadas pela automontagem de proteínas estruturais virais, apresentam segurança e imunogenicidade, tornando-as indispensáveis para a pesquisa de vacinas e sistemas de administração de medicamentos.

Tanto os vírus quanto as VLPs servem como ferramentas essenciais em investigações científicas fundamentais destinadas a elucidar mecanismos celulares e descobrir estratégias terapêuticas inovadoras.
Tecnologia Exodus H-600
O Exodus H-600, desenvolvido pela Exodus Bio, é capaz de eliminar rapidamente impurezas — como ácidos nucleicos livres e proteínas — das amostras, ao mesmo tempo em que retém vírus e VLPs com eficiência, prevenindo agregação de partículas e entupimento de membrana durante o processo. Ao empregar purificação de baixa força de cisalhamento, garante produtos-alvo com alta pureza e atividade biológica, aumentando a eficiência experimental e a consistência dos resultados.

Aplicação do Exodus H-600 na Purificação e Enriquecimento de Vírus e VLPs
Esta nota de aplicação apresenta os resultados experimentais documentados pela Exodus Bio para purificação de vírus e VLPs com o H-600, seguidos de contexto técnico sobre desafios de purificação viral, princípio de operação do equipamento e aplicações documentadas.
- Resultados: caracterização estrutural por TEM
- Resultados: recuperação de vetores lentivirais
- Desafios técnicos na purificação de vírus e VLPs
- Princípio de operação do Exodus H-600
- Aplicações documentadas
- FAQ
Caso 1: Purificação de Vírus e VLPs: Caracterização por Microscopia Eletrônica de Transmissão (TEM)
A Exodus Bio documentou a caracterização por microscopia eletrônica de transmissão (TEM) de três tipos de partículas purificadas com o Exodus H-600, demonstrando preservação de morfologia típica em cada caso.

Bacteriófagos
As imagens de TEM revelam morfologia típica e preservada, com estruturas de cabeça e cauda íntegras. A preservação dessas estruturas é essencial para aplicações em fagoterapia e estudos de interação fago-hospedeiro.
Partículas de automontagem de proteínas de fagos
As VLPs apresentaram morfologia esférica uniforme, sem evidência de agregação ou colapso estrutural, indicando que o processo de baixo cisalhamento manteve a integridade das partículas ocas.
RFV
O vírus da Febre do Vale do Rift, arbovírus de relevância em saúde pública e objeto de pesquisa em vacinas, foi isolado e caracterizado com morfologia preservada. A resolução das imagens confirma adequação do processo para análise estrutural de partículas nessa faixa de tamanho.
A preservação da morfologia viral após purificação é um indicador direto de que o método não induziu desnaturação proteica nem ruptura de envelope — condição necessária para que estudos estruturais e funcionais subsequentes produzam dados válidos.
Caso 2: Recuperação de Vetores Lentivirais após Purificação com Exodus H-600
Os vetores lentivirais são ferramentas centrais em terapia gênica e edição genômica por sua capacidade de integração estável no genoma de células em divisão e quiescentes. A eficiência de purificação é avaliada por dois parâmetros complementares: o título infeccioso (partículas funcionalmente ativas) e o título físico (total de partículas, ativas ou não).
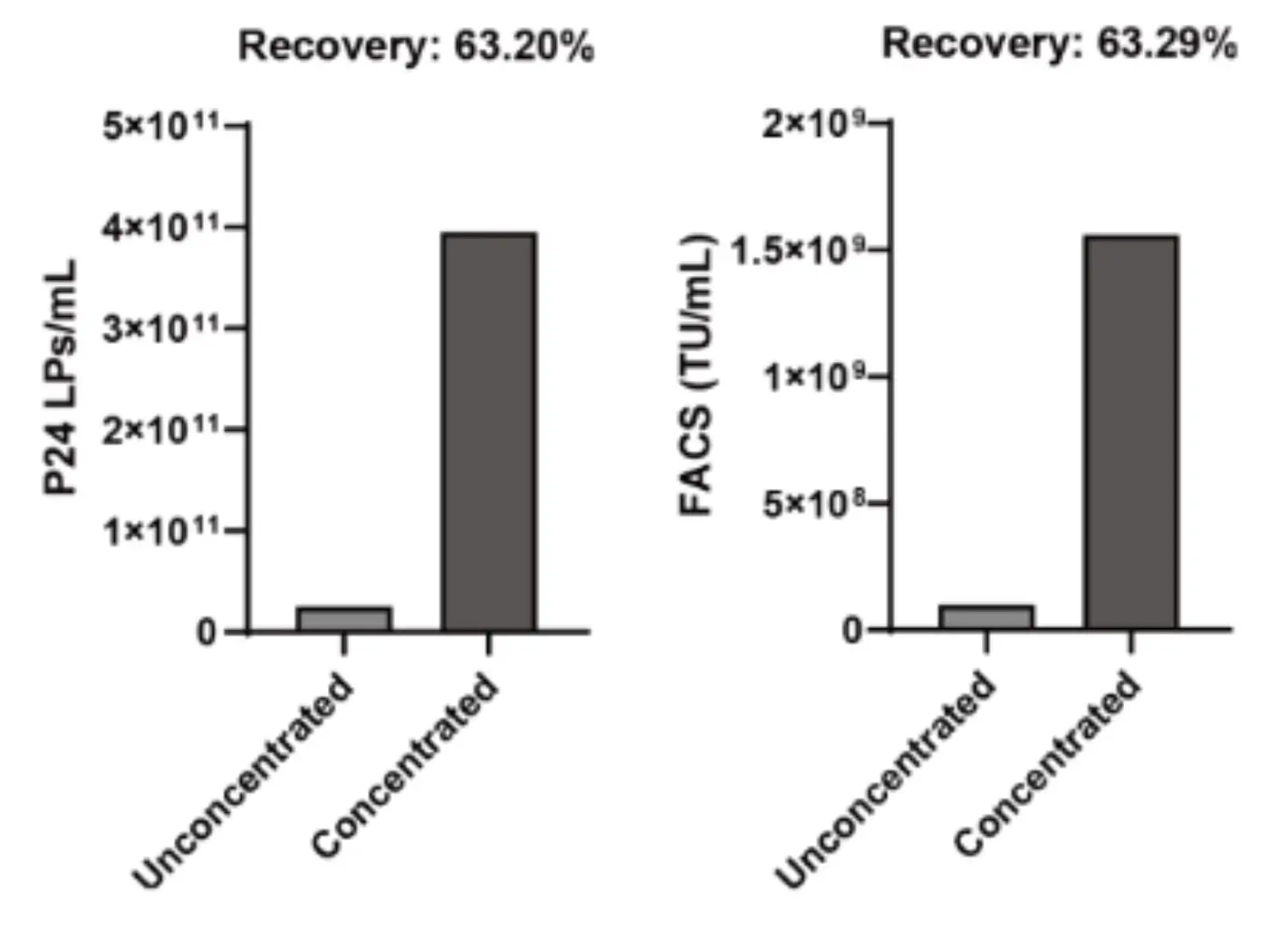
A taxa de recuperação de ~63% é consistente com a faixa reportada na literatura para purificação de vetores lentivirais em etapas individuais, métodos baseados em TFF e cromatografia AEX reportam recuperações entre 20–80% dependendo do protocolo e escala.
O dado mais relevante é a equivalência entre as taxas de recuperação infecciosa (63,29%) e física (63,0%): em métodos que causam dano estrutural, a recuperação de título físico tende a superar a de título infeccioso, refletindo enriquecimento de partículas defeituosas.
A proporção próxima de 1 observada indica que o processo preservou a funcionalidade das partículas recuperadas, conforme documentado pela Exodus Bio.
Desafios Técnicos na Purificação de Vírus e VLPs
Impurezas e complexidade da matriz amostral
Vírus e VLPs coexistem nas amostras com impurezas de tamanho e massa molecular variados: ácidos nucleicos livres, proteínas do hospedeiro, agregados proteicos e debris celulares. A separação seletiva dessas impurezas sem degradar a partícula viral é o problema central de qualquer processo de purificação nesse contexto.
Limitações dos métodos convencionais
Métodos convencionais como a ultracentrifugação em gradiente de sacarose e a cromatografia de troca iônica oferecem pureza razoável, mas apresentam limitações conhecidas: força de cisalhamento elevada, risco de agregação de partículas, tempo de processamento longo e dificuldade de escalonamento. Sistemas de filtração com fluxo unidirecional resultam em entupimento progressivo da membrana e perda de rendimento.
Comparações documentadas pelo fabricante mostram superioridade do Exodus H-600 em pureza e rendimento para EVs frente à ultracentrifugação, com remoção de proteínas superior a 99%.
Para vírus, os dados disponíveis focam na preservação de integridade estrutural (TEM) e na equivalência entre títulos infeccioso e físico; comparações quantitativas diretas com outros métodos de purificação viral estão limitadas aos casos documentados pelo fabricante.
Atividade biológica como critério de qualidade
Para vetores virais usados em terapia gênica, partículas fisicamente intactas mas funcionalmente inativas inflariam o título físico sem correspondência no título infeccioso, comprometendo dose, eficácia e reprodutibilidade experimental. A preservação da atividade biológica durante a purificação é, portanto, tão crítica quanto a remoção de impurezas.
Princípio de Operação do Exodus H-600
O Exodus H-600 opera por nanofiltração de membrana dupla integrada a dois mecanismos de oscilação simultâneos, conforme especificação técnica da Exodus Bio:
- NPO (Negative Pressure Oscillation): oscilação periódica de pressão negativa que mobiliza o fluido de forma controlada, reduzindo o acúmulo de material na superfície da membrana e prevenindo entupimento progressivo.
- HO (Double-Coupled Ultrasonic Harmonic Oscillations): oscilações harmônicas ultrassônicas acopladas que mantêm as partículas em suspensão homogênea, prevenindo agregação durante o processo.
Esses dois mecanismos combinados permitem que ácidos nucleicos livres e proteínas sejam removidos continuamente, enquanto vírus e VLPs — retidos pela membrana nanoporosa em função do tamanho — são concentrados e enriquecidos. O processo ocorre com força de cisalhamento reduzida, determinante para preservar a atividade biológica das partículas.
Vale notar que o Exodus H-600 é primariamente projetado para o isolamento de exossomos e vesículas extracelulares (EVs), alcançando pureza aproximada de 99% e rendimento de ~90% em diversos biofluidos, conforme documentado pela Exodus Bio. A purificação de vírus e VLPs é uma das aplicações-chave do sistema, com dados experimentais publicados pelo fabricante para as amostras descritas nesta nota.
Principais especificações técnicas do H-600:
- Volume de amostra: 10 µL a 250 mL
- Velocidade máxima de processamento: 200 mL/h
- Temperatura do reservatório: 2–8 °C
- Tamanhos de dispositivo de isolamento: S, M e L
- Display: tela touch de 10,4" com monitoramento em tempo real
- Esterilização UV interna com desligamento automático após 30 min
- Capacidade de registro: até 20.000 isolamentos
Outras Aplicações Documentadas do Exodus H-600
Além do isolamento de exossomos e vesículas extracelulares, o Exodus H-600 tem aplicações validadas em diferentes biofluidos e contextos clínicos. Seu mecanismo de dupla membrana com baixo cisalhamento preserva a integridade das partículas, viabilizando análises multi-ômicas de alta resolução. Os estudos abaixo ilustram a versatilidade do sistema em pesquisa translacional e diagnóstico não invasivo.
- Exossomos urinários: Isolamento de alta pureza para rastreamento transcriptômico de origens teciduais, com potencial diagnóstico em câncer renal e de bexiga (PNAS, 2021).
- Vesículas extracelulares em lágrimas: Isolamento rápido a partir de microlitros de amostra para análise proteômica e de miRNAs em doenças oculares como olho seco e retinopatia diabética (ACS Nano, 2022; Science Advances, 2023).
- Exossomos plasmáticos — transcriptômica e metabolômica: Identificação de biomarcadores como MIF e TUBA1B em pancreatite aguda grave via análise integrada de RNAs longos e metabólitos (Clinical and Translational Medicine, 2022).
- Exossomos plasmáticos — fingerprinting proteômico: Perfis proteômicos diferenciais por MALDI-TOF para diagnóstico não invasivo de pancreatite aguda (ACS Nano, 2023).
- Vírus e VLPs: Purificação com preservação estrutural e funcional, validada pelo fabricante para partículas maiores que exossomos.
FAQ — Perguntas Frequentes sobre o Exodus H-600 na Purificação de Vírus
O que é o Exodus H-600?
É um sistema automático de nanofiltração de membrana dupla desenvolvido pela Exodus Bio, otimizado primariamente para o isolamento de exossomos e vesículas extracelulares (EVs), com aplicação documentada também para vírus e VLPs. Utiliza oscilação de pressão negativa (NPO) e oscilações harmônicas ultrassônicas (HO) para remover impurezas e concentrar as partículas de interesse a partir de amostras biológicas.
Qual a diferença entre título infeccioso e título físico em vetores virais?
O título físico contabiliza todas as partículas virais presentes na amostra, independentemente de serem funcionais. O título infeccioso mede apenas as partículas capazes de infectar células-alvo. A razão entre os dois é um indicador direto da qualidade do processo de purificação.
O que significa purificação por baixo cisalhamento?
Cisalhamento (shear force) é a força mecânica aplicada ao fluido durante o processamento. Métodos de alto cisalhamento, como a ultracentrifugação, podem romper partículas frágeis ou desnaturar proteínas de superfície. O baixo cisalhamento do H-600 reduz esse risco, preservando estrutura e função das partículas.
O Exodus H-600 é adequado para purificação de vetores AAV?
O site da Exodus Bio documenta aplicações com lentivírus, bacteriófagos e VLPs. Aplicações com AAV não estão documentadas publicamente até o momento. Outros vetores podem ser compatíveis pelo mecanismo de baixo cisalhamento e retenção por tamanho, mas isso não foi verificado publicamente. Recomenda-se consulta direta ao fabricante para essa aplicação específica.
Como o sistema previne o entupimento da membrana?
A oscilação periódica de pressão negativa (NPO) mobiliza continuamente o fluido na interface da membrana, impedindo o acúmulo progressivo de material — fenômeno conhecido como fouling — limitação comum em sistemas de filtração tangencial convencional.
Quais impurezas são removidas durante a purificação com o Exodus H-600?
Ácidos nucleicos livres e proteínas são as principais impurezas eliminadas. O tamanho dessas moléculas, inferior ao das partículas virais, permite que atravessem a membrana nanoporosa enquanto vírus e VLPs são retidos e concentrados.
Qual o volume máximo de amostra que o H-600 processa?
O Exodus H-600 processa volumes de 10 µL a 250 mL, com velocidade máxima de 200 mL/h, conforme especificação técnica do fabricante.
O Exodus H-600 está disponível no Brasil?
Sim. O Exodus H-600 é distribuído no Brasil pela Dafratec, distribuidora especializada em equipamentos científicos de alta precisão para bioprocessos, análise de partículas e caracterização de materiais.
Leitura Recomendada
- Partículas Semelhantes a Vírus (VLPs) — estrutura, produção e aplicações em vacinas
- Vetores Lentivirais em Terapia Gênica — produção, titulação e purificação
- Exossomos e Vesículas Extracelulares — isolamento e caracterização
Fale com nossa equipe
Tire suas dúvidas sobre o Exodus H-600 e descubra como ele se aplica ao seu contexto de pesquisa.
Falar com nossa equipe