O gargalo bilionário da indústria biofarmacêutica e as ferramentas para superá-lo
O scale-up de bioprocessos representa um dos maiores desafios técnicos e econômicos da indústria biofarmacêutica moderna. A transição de cultivos em escala de laboratório para produção industrial envolve uma complexa interação entre variáveis biológicas, físico-químicas e de engenharia que frequentemente resultam em perda de rendimento, qualidade inconsistente e atrasos significativos no time-to-market.
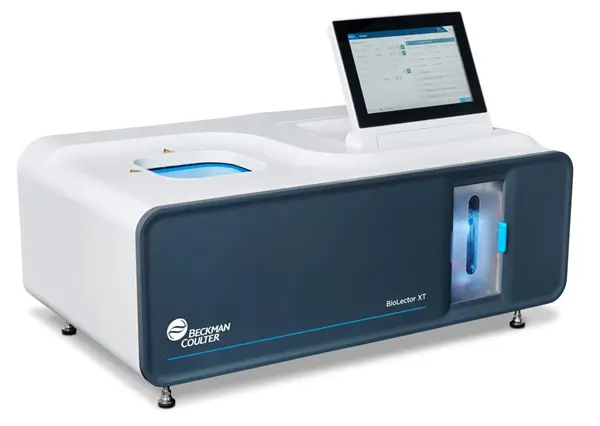
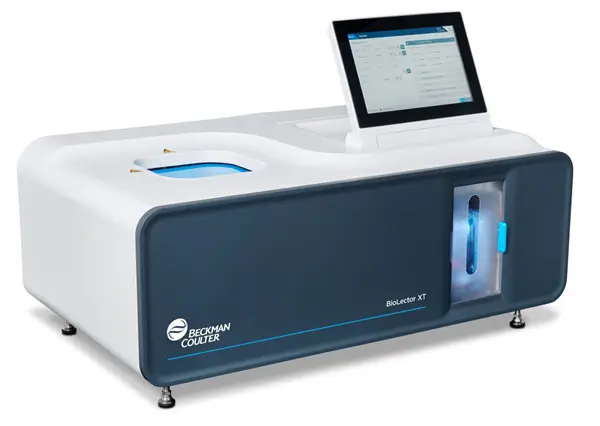
Conheça o BioLector XT da Beckman Coulter com 48 microbiorreadores paralelos simultâneos disponíveis e controle ativo de pH individualizado por poço. Saiba mais sobre esse Microbiorreator
Segundo estudo publicado no MAbs Journal , o custo capitalizado de P&D para levar um novo biofármaco ao mercado subiu de US$ 1,2 bilhão em 2007 para aproximadamente US$ 2,8 bilhões em 2016, com taxas de sucesso da Fase I à aprovação caindo de 30% para 12%.
Este cenário evidencia a necessidade urgente de ferramentas que acelerem o desenvolvimento de processos, reduzam custos e aumentem a previsibilidade do scale-up — contexto onde os microbiorreatores de alta vazão emergem como tecnologia transformadora.
Neste artigo, você encontrará:
- Os principais desafios técnicos do scale-up em bioprocessos
- Por que o screening tradicional falha em prever o desempenho industrial
- Como microbiorreatores resolvem a lacuna entre laboratório e produção
- Evidências científicas de transferibilidade de dados em microescala
- Aplicações práticas na indústria biofarmacêutica
O Que É Scale-Up de Bioprocessos e Por Que É Tão Desafiador?
O scale-up refere-se ao processo de aumentar o volume de produção mantendo as características críticas do processo e do produto. Na prática, isso significa transferir um processo otimizado em biorreatores de bancada (1-10L) para reatores piloto (50-500L) e, finalmente, para escala de produção (1.000-20.000L ou mais).
Conforme descrito em revisão publicada na Trends in Biotechnology , os biorreatores miniaturizados estão ganhando popularidade como abordagem custo-efetiva para experimentação em scale-down, porém replicar com precisão as condições do processo em grande escala permanece desafiador.
Heterogeneidade de Parâmetros em Grande Escala
Em escala laboratorial, parâmetros como temperatura, pH e suprimento de nutrientes podem ser rigidamente controlados, garantindo condições ótimas para crescimento celular e formação de produto. Entretanto, o scale-up frequentemente leva à heterogeneidade desses parâmetros, o que pode afetar a qualidade e o rendimento do produto.
Os principais desafios técnicos incluem:
- Transferência de oxigênio (k L a): Em biorreatores grandes, a taxa de transferência de oxigênio pode se tornar fator limitante devido à redução da relação superfície/volume. O k L a típico em escala de bancada (200-400 h -1 ) é difícil de reproduzir em escalas maiores sem aumento significativo de potência de agitação.
- Estresse de cisalhamento: A velocidade de ponta do impelidor (tip speed) aumenta com o diâmetro do reator. Células sensíveis, especialmente linhagens de mamíferos e alguns fungos filamentosos, podem sofrer danos mecânicos que comprometem viabilidade e produtividade.
- Gradientes de nutrientes: O tempo de mistura (mixing time) aumenta de segundos em escala de bancada para minutos em reatores industriais, criando zonas de alta e baixa concentração de substrato que afetam metabolismo celular.
- Controle de pH: A adição pontual de base/ácido cria gradientes locais de pH que podem exceder 2 unidades antes da homogeneização, causando estresse celular e impactando qualidade de produto.
- Transferência de calor: A razão superfície/volume diminui com o aumento de escala, dificultando a remoção de calor metabólico e exigindo sistemas de resfriamento mais robustos.
Critérios Clássicos de Scale-Up e Suas Limitações
Tradicionalmente, o scale-up é realizado mantendo constantes um ou mais parâmetros adimensionais:
| Critério | Parâmetro Mantido Constante | Limitação Principal |
|---|---|---|
| Potência por volume (P/V) | W/m³ | Não garante mesmo k L a ou mixing time |
| Velocidade de ponta | πND (m/s) | Pode resultar em cisalhamento excessivo |
| k L a constante | h -1 | Requer aumento desproporcional de potência |
| Tempo de mistura | segundos | Frequentemente impraticável em grande escala |
| Número de Reynolds | Re = ρND²/μ | Regime turbulento já garantido em escalas maiores |
A realidade é que nenhum critério único é universalmente aplicável . A escolha depende do processo específico e dos parâmetros críticos identificados durante desenvolvimento.
O Problema do Screening Tradicional: A Desconexão Entre Laboratório e Produção
Historicamente, o screening de cepas e condições de processo é realizado em shake flasks ou microplacas operando em modo batch. Esta abordagem, embora permita alto throughput, cria condições significativamente diferentes daquelas encontradas em processos de produção real.
Segundo estudo publicado na Scientific Reports , o cultivo em shake flask, método tradicional de screening, permite paralelização, mas automação limitada e intensidade de trabalho restringem severamente sua aplicação eficiente em contextos de alta vazão.
Limitações Críticas do Screening em Batch
As principais limitações técnicas incluem:
- Ausência de controle de pH: Células crescem sob acidificação progressiva do meio (típico: pH 7.0 → 5.5 em culturas de E. coli ), alterando expressão gênica e atividade enzimática.
- Taxas de crescimento máximas (μ max ): Sem limitação de carbono, células crescem em velocidade máxima, muito diferente do μ controlado (0.1-0.2 h -1 ) típico de processos industriais.
- Metabolismo overflow: Altas concentrações de substrato (>1 g/L glicose para E. coli ) desencadeiam formação de acetato via metabolismo overflow, mesmo em condições aeróbicas.
- Limitação de oxigênio: O k L a em shake flasks (40-200 h -1 ) frequentemente é insuficiente para altas densidades celulares, resultando em culturas limitadas por O₂.
- Dados offline limitados: Apenas medições de ponto final (OD, título de produto), sem cinética de crescimento ou produção.
Conforme destacado por Neubauer e colaboradores em estudo publicado na Microbial Cell Factories , realizar o screening já em condições de fed-batch limitaria a quantidade de trabalho e garantiria que as condições selecionadas também funcionem na escala de produção.
O Problema da Seleção Enviesada
Um aspecto frequentemente negligenciado é que o melhor clone em condições batch raramente é o melhor clone em condições fed-batch . Isso ocorre porque:
- Clones com alta μ max podem ter baixa produtividade específica em condições de crescimento limitado
- A resposta ao estresse metabólico (baixa disponibilidade de substrato) varia entre clones
- Mecanismos de secreção e folding proteico são afetados diferentemente pela taxa de crescimento
- A estabilidade plasmidial sob diferentes regimes metabólicos é variável
Resultados de otimização em microplacas ou shake flasks frequentemente não são diretamente transferíveis para escala de biorreator e produção industrial, onde o objetivo é maximizar o rendimento de produto por litro.
Microbiorreatores: Fechando a Lacuna Entre Desenvolvimento e Produção Industrial
Os microbiorreatores representam uma evolução fundamental nas ferramentas de desenvolvimento de bioprocessos. Diferentemente de shake flasks e microplacas convencionais, esses sistemas combinam o alto throughput da miniaturização com capacidades de monitoramento e controle similares às encontradas em biorreatores de bancada.
Conforme revisão publicada na Biotechnology Journal , sistemas de microbiorreatores permitem o desenvolvimento acelerado de bioprocessos ao fornecer controle preciso sobre parâmetros críticos em volumes de microlitros.
Evolução Tecnológica: De Microplacas a Microbiorreatores
A evolução pode ser traçada em gerações:
- 1ª Geração: Microplacas convencionais (96/384 wells) — apenas crescimento batch, sem monitoramento
- 2ª Geração: Microplacas com sensores ópticos (pH, DO) — monitoramento online, mas sem controle
- 3ª Geração: Sistemas com liberação enzimática de substrato — fed-batch passivo, sem feedback
- 4ª Geração: Microbiorreatores com microfluídica — controle ativo de pH e feeding com feedback em tempo real
Características Essenciais dos Microbiorreatores Modernos
Os sistemas avançados de microbiorreatores oferecem:
- Monitoramento online em tempo real: Biomassa (por dispersão de luz), pH (optodos), oxigênio dissolvido (optodos) e múltiplos canais de fluorescência (GFP, mCherry, NADH, riboflavina)
- Cultivos paralelos massivamente: Até 48 experimentos simultâneos em uma única corrida, possibilitando DoE completo
- Modo fed-batch verdadeiro: Liberação controlada de substrato (enzimática ou microfluídica) mimetizando condições industriais
- Controle microfluídico: Dosagem precisa em escala de nanolitros para pH e feeding individualizado por poço
- Sensores ópticos pré-calibrados: Placas descartáveis prontas para uso, eliminando calibração manual e risco de contaminação cruzada
- Controle atmosférico: Gassing individualizado para estudos aeróbicos, microaeróbicos e anaeróbicos
Vantagens Quantificáveis
| Parâmetro | Shake Flask | Biorreator Bancada | Microbiorreator |
|---|---|---|---|
| Throughput (experimentos/semana) | 20-50 | 4-8 | 200-500 |
| Volume por experimento | 50-500 mL | 1-10 L | 0.5-1.5 mL |
| Consumo de meio/experimento | ~250 mL | ~5 L | ~1 mL |
| Dados online | Não | Sim | Sim |
| Controle de pH | Não | Sim | Sim (microfluídico) |
| Modo fed-batch | Limitado | Sim | Sim |
| Custo relativo/experimento | Baixo | Alto | Muito baixo |
Evidências Científicas: Transferibilidade de Dados do Microbiorreator
A questão central para qualquer plataforma de screening é: os resultados obtidos em pequena escala são transferíveis para escalas maiores? Estudos recentes demonstram consistentemente que microbiorreatores bem projetados fornecem dados altamente preditivos.
Estudo de Caso 1: Produção de Fragmentos Fab em E. coli
Um estudo abrangente publicado na Scientific Reports (Fink et al., 2021) avaliou a transferibilidade de resultados de screening em microbiorreator BioLector para biorreatores de bancada (1.2L) e produção em alta densidade celular (30L STR).
Metodologia:
- 22 combinações diferentes de hospedeiro ( E. coli BL21(DE3), HMS174(DE3), RV308(DE3))
- 4 fragmentos Fab diferentes (FTN2, BIWA4, BIBH1, Fabx)
- 2 sequências sinal (ompASS, dsbASS)
- Sistemas de expressão genômica integrados e plasmidiais
- Cultivo fed-batch em microbiorreator com liberação enzimática de glicose
Resultados principais:
- Rankings idênticos: A classificação de clones baseada em rendimento específico (mg Fab/g CDM) foi reproduzida nos biorreatores de bancada em 15 de 16 combinações
- Ranking de Fabs preservado: FTN2 > BIWA4 > BIBH1 > Fabx em todas as combinações hospedeiro/líder
- Efeito de hospedeiro consistente: HMS174(DE3) superou BL21(DE3) em rendimento específico em ambas as escalas
- Efeito de sequência sinal: ompASS resultou em maiores títulos que dsbASS, confirmado em escala maior
Estudo de Caso 2: Otimização de Bioprocesso com Integração Robótica
Estudo publicado na Microbial Cell Factories (Rohe et al., 2012) demonstrou a integração de microbiorreator BioLector com liquid handler para otimização automatizada de processos.
Resultados:
- Todos os parâmetros otimizados em microescala foram perfeitamente escaláveis para biorreatores de 1L e 20L
- Aumento de throughput de 2 ordens de magnitude comparado a biorreatores convencionais
- Estatística robusta com replicatas técnicas e biológicas em cada condição
- Redução de 80% no tempo de desenvolvimento de processo
Estudo de Caso 3: Screening Fed-Batch em Microplacas de 96 Poços
Trabalho publicado na Microbial Cell Factories (Krause et al., 2010) demonstrou pela primeira vez screening multifatorial de bibliotecas de clonagem combinado com técnica fed-batch em microplacas.
Achados principais:
- Screening de 45 vetores de expressão citoplasmática para proteína de difícil expressão (inibidor de RNase)
- Condições otimizadas em microescala foram reproduzidas em biorreatores de 10L
- Identificação de combinações promotor/RBS/fusão ótimas impossível com métodos tradicionais devido ao número de experimentos necessários
Aplicações Práticas na Indústria Biofarmacêutica
Os microbiorreatores encontram aplicação em diversas etapas do desenvolvimento de bioprocessos, cada uma com requisitos específicos:
1. Screening de Cepas e Clones
A avaliação inicial de bibliotecas de clones pode ser realizada de forma sistemática, testando simultaneamente:
- Cepas hospedeiras: Comparação de backgrounds genéticos (K-12 vs B, protease-deficientes, chaperone-coexpressantes)
- Sistemas de expressão: Plasmídeo vs integração genômica, número de cópias, estabilidade
- Promotores: Força, regulação (lac, tac, T7, araBAD, rhaBAD), vazamento basal
- Sequências sinal: Via Sec (ompA, pelB, phoA) vs via SRP (dsbA, torA) para secreção periplasmática
- Tags de fusão: Impacto em solubilidade, folding e rendimento
2. Otimização de Meio de Cultura (Media Screening)
Com capacidade para 48 cultivos paralelos, metodologias de Design of Experiments (DoE) podem ser aplicadas para:
- Screening de fontes de carbono: Glicose, glicerol, lactose, galactose e misturas
- Fontes de nitrogênio: Sais de amônio, aminoácidos, hidrolisados, extrato de levedura
- Elementos traço: Otimização de formulação de micronutrientes
- Suplementos específicos: Precursores, indutores, chaperones químicos
- Resposta de superfície: Identificação de interações entre componentes
3. Desenvolvimento de Estratégias de Feeding
O modo fed-batch em microescala permite testar diferentes estratégias antes da transferência:
- Perfis de alimentação: Linear, exponencial, constante, baseado em DO
- Taxas de crescimento alvo: Identificação do μ ótimo para produção
- Estratégias de indução: Momento, concentração de indutor, temperatura pós-indução
- Relação C/N: Otimização da razão carbono/nitrogênio durante produção
4. Caracterização de Processos e QbD
A coleta contínua de dados online possibilita:
- Identificação de CPPs: Parâmetros Críticos de Processo com significância estatística
- Definição de Design Space: Espaço operacional comprovado para qualidade consistente
- Modelos cinéticos: Construção de modelos preditivos para crescimento e produção
- Análise de sensibilidade: Avaliação de robustez do processo
O BioLector XT: Especificações Técnicas e Capacidades
O BioLector XT da Beckman Coulter Life Sciences representa o estado da arte em tecnologia de microbiorreatores, incorporando as características essenciais para screening preditivo e desenvolvimento acelerado de bioprocessos.
Especificações do Sistema
Não, essa tabela é sobre critérios de scale-up (engenharia de bioprocessos em geral). As informações do brochure iriam na tabela de especificações do BioLector XT, que está mais abaixo no artigo. Aqui está ela corrigida e enriquecida:| Característica | Especificação |
|---|---|
| Formato de placa | 48 ou 32 poços FlowerPlate (padrão ANSI/SLAS) |
| Volume de trabalho | 800–2400 µL por poço |
| Monitoramento de biomassa | Dispersão de luz (faixa: até 250 OD 600 / 50 g/L CDW, sem diluição) |
| Monitoramento de pH | Optodos pré-calibrados (faixa: 5.0–7.5 ou 4–6 com módulo low pH) |
| Monitoramento de DO | Optodos pré-calibrados (faixa: 0–100% saturação) |
| Canais de fluorescência | Até 6 filtros configuráveis (GFP, YFP, DsRed, NAD(P)H, riboflavina) |
| Controle de O₂ | 1–100% (módulo anaeróbico: cultivo estritamente anaeróbico) |
| Controle de CO₂ | 0–12% |
| k L a | 30–600 h -1 |
| Agitação | 100–1500 rpm orbital (shaker 3 mm) |
| Temperatura | 8°C abaixo da ambiente até 50°C |
| Tempo de leitura | ~2.7 min/parâmetro/48 poços |
| Integração | Compatível com robôs liquid handling (automação) |
| Compliance | Ferramenta para PAT e QbD |
Módulo Microfluídico
O módulo opcional de microfluídica permite:
- Controle de pH individualizado: Por poço, usando reservatórios dedicados
- Feeding individualizado: Perfis programáveis para cada cultivo
- Dosagem em nanolitros: Via microválvulas integradas na placa
- Configuração 2:4: 2 reservatórios para cada 4 poços de cultivo
- Placas descartáveis: Pré-esterilizadas por radiação gama, prontas para uso
Módulo Anaeróbico
Para organismos sensíveis ao oxigênio:
- Controle de O₂ abaixo de 0.1%
- Ideal para probióticos ( Lactobacillus , Bifidobacterium )
- Estudos de bactérias produtoras de solventes ( Clostridium )
- Processos de fermentação anaeróbica
Módulo de Luz (LAM - Light Array Module)
Para organismos fototróficos:
- Espectro de 400-700 nm (PAR)
- 16 tipos de LEDs controláveis individualmente
- Irradiância até 3500 µmol/m²/s
- Aplicações: microalgas, cianobactérias, culturas fotomixotróficas
Integração com Automação
A integração do BioLector XT com liquid handlers (Biomek i5/i7) permite:
- Inoculação automatizada baseada em OD
- Indução triggerd por biomassa ou tempo
- Amostragem automatizada sem interrupção de agitação
- Dosagem de feeds ou aditivos em resposta a sinais online
- Workflows de DoE completamente automatizados
FAQ — Perguntas Frequentes sobre Scale-Up de Bioprocessos
O que é scale-up de bioprocessos?
É o processo de aumentar o volume de produção biofarmacêutica mantendo as características críticas do processo e qualidade do produto, transferindo de escala laboratorial (litros) para escala industrial (milhares de litros). Envolve ajustes em parâmetros de engenharia para compensar diferenças em transferência de massa, calor e mistura entre escalas.
Por que o scale-up é considerado um gargalo na indústria biofarmacêutica?
Porque a transição de escala frequentemente resulta em perda de rendimento (20-50% não é incomum), qualidade inconsistente e falhas de processo. Isso ocorre devido às diferenças fundamentais em k L a, gradientes de nutrientes, tempo de mistura e estresse de cisalhamento entre escalas. Cada falha de scale-up pode custar meses de atraso e milhões em investimento perdido.
Qual a diferença entre screening em batch e fed-batch?
No modo batch , todos os nutrientes são adicionados no início e as células crescem em μ max até esgotamento do substrato. No fed-batch , o substrato é adicionado de forma controlada durante o cultivo, mantendo baixa concentração residual e permitindo crescimento em taxa controlada. Fed-batch mimetiza condições industriais e evita metabolismo overflow (formação de acetato em E. coli , etanol em leveduras).
Como os microbiorreatores aceleram o desenvolvimento de bioprocessos?
Permitem testar 48+ condições simultaneamente com monitoramento em tempo real (biomassa, pH, DO, fluorescência), gerando dados transferíveis para escalas maiores. O consumo de meio é ~1 mL/experimento vs ~5L em biorreatores de bancada. Isso reduz custo em >90% e tempo de desenvolvimento em 50-80%, permitindo DoE completo em dias ao invés de meses.
Os resultados obtidos em microbiorreatores são realmente transferíveis para produção industrial?
Estudos científicos demonstram alta transferibilidade (>90% concordância em rankings de clones) quando o microbiorreator opera em condições que mimetizam o processo industrial — especialmente em modo fed-batch com controle de taxa de crescimento. A chave é garantir que os parâmetros críticos (μ, pH, DO) sejam similares entre escalas. Validação com subset de clones em biorreator de bancada é recomendada.
Quais parâmetros podem ser monitorados em tempo real no BioLector XT?
Biomassa (dispersão de luz, correlacionável com OD e CDM), pH (optodo, faixa 5.0-7.5 ou 4-6 (low pH module)), oxigênio dissolvido (optodo, 0-100% saturação) e até 6 canais de fluorescência customizáveis para GFP/YFP/mCherry (expressão), NADH (estado metabólico), riboflavina (estresse), PI (viabilidade), entre outros. Frequência de aquisição: até cada 3 minutos por poço.
O BioLector XT pode ser usado para organismos anaeróbicos?
Sim, o módulo anaeróbico permite controle de O₂ abaixo de 0.1% (praticamente anóxico), adequado para cultivo de probióticos ( Lactobacillus , Bifidobacterium ), Clostridium para produção de solventes, e outros organismos estritamente anaeróbicos. O sistema também suporta condições microaeróbicas (0.5-5% O₂) para processos como produção de ácido láctico.
Considerações para Implementação
Quando Usar Microbiorreatores vs Biorreatores de Bancada
Microbiorreatores são ideais para:
- Screening inicial de >20 condições/clones
- DoE para otimização de meio ou condições de processo
- Estudos de cinética de crescimento e produção
- Avaliação preliminar de robustez de processo
Biorreatores de bancada permanecem necessários para:
- Validação de condições selecionadas em microescala
- Geração de material para caracterização analítica extensiva
- Estudos de scale-up com critérios de engenharia específicos
- Processos que requerem volumes >2 mL por condição
Boas Práticas para Maximizar Transferibilidade
- Usar modo fed-batch: Evitar screening batch para processos fed-batch industriais
- Controlar taxa de crescimento: Mimetizar o μ do processo alvo (tipicamente 0.1-0.2 h -1 )
- Incluir controles de referência: Clone/condição de referência em cada placa para normalização
- Validar em escala intermediária: Confirmar top hits em biorreator de bancada antes de scale-up maior
- Documentar completamente: Registrar todos os parâmetros para reprodutibilidade
Conclusão
O scale-up de bioprocessos permanece como um dos desafios mais significativos no desenvolvimento biofarmacêutico, impactando diretamente custos, prazos e probabilidade de sucesso de novos produtos. A desconexão entre condições de screening tradicionais (batch em shake flasks) e produção industrial (fed-batch controlado) é uma fonte importante de falhas e retrabalho.
A adoção de plataformas de microbiorreatores que operem em condições representativas da produção industrial oferece um caminho comprovado para:
- Reduzir riscos de scale-up através de screening mais preditivo
- Acelerar desenvolvimento de processo em 50-80%
- Reduzir custos de desenvolvimento em >90%
- Permitir exploração sistemática de espaço de design via DoE
- Gerar dados de qualidade para suporte a QbD e submissões regulatórias
As evidências científicas demonstram consistentemente que dados gerados em microbiorreatores bem projetados, como o BioLector XT, são transferíveis para escalas maiores, permitindo decisões mais assertivas já nas fases iniciais do desenvolvimento.
Acelere seu Desenvolvimento de Bioprocessos
A Dafratec, como representante oficial da Beckman Coulter Life Sciences no Brasil, oferece consultoria especializada para implementação de soluções de microbiorreatores adaptadas às necessidades específicas de cada projeto.
Referências Científicas Citadas
- Fink M, et al. (2021). High-throughput microbioreactor provides a capable tool for early stage bioprocess development. Scientific Reports 11:2056. DOI: 10.1038/s41598-021-81633-6
- Krause M, et al. (2010). Novel approach of high cell density recombinant bioprocess development. Microbial Cell Factories 9:35. DOI: 10.1186/1475-2859-9-35
- Rohe P, et al. (2012). An automated workflow for enhancing microbial bioprocess optimization. Microbial Cell Factories 11:144. DOI: 10.1186/1475-2859-11-144
- Hemmerich J, et al. (2018). Microbioreactor systems for accelerated bioprocess development. Biotechnology Journal 13:1700141. DOI: 10.1002/biot.201700141
- Maruthamuthu MK, et al. (2020). Benchmarking biopharmaceutical process development and manufacturing cost contributions to R&D. MAbs 12:1754999. DOI: 10.1080/19420862.2020.1754999
- Tajsoleiman T, et al. (2019). An industrial perspective on scale-down challenges using miniaturized bioreactors. Trends in Biotechnology 37:697-706. DOI: 10.1016/j.tibtech.2019.01.002
Leituras Relacionadas
- Design of Experiments (DoE) aplicado ao desenvolvimento de bioprocessos
- Estratégias de fed-batch para expressão de proteínas recombinantes em E. coli
- Quality by Design (QbD) na manufatura biofarmacêutica