Os avanços na engenharia de bioprocessos têm impulsionado a pesquisa com microalgas, como Chlorella vulgaris , para diversas aplicações, incluindo produção de biocombustíveis, sequestro de CO₂ e biorremediação ambiental .
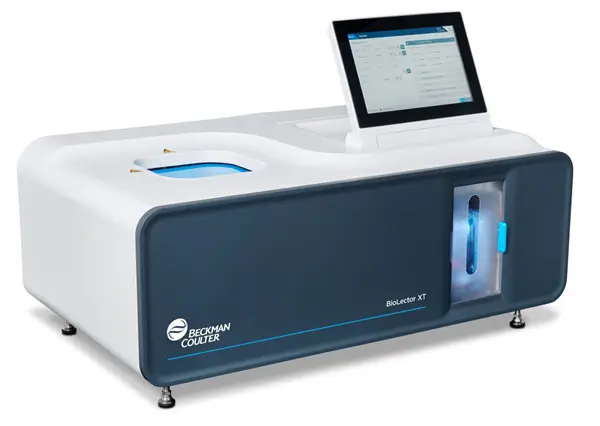
Este artigo explora os desafios e soluções para o cultivo eficiente de Chlorella vulgaris, destacando o uso do microbioreator BioLector XT, equipado com o módulo de iluminação LAM (Light Array Module), que permite o controle preciso da iluminação e monitoramento contínuo de variáveis essenciais como biomassa, clorofila e pH. Além disso, são apresentados métodos de calibração de sensores ópticos e estratégias de cultivo fotoautotrófico, visando a maximização da produtividade da biomassa.
Desafios para a Aplicação Industrial de Microalgas
O uso de microalgas como fábricas celulares microbianas oferece soluções para desafios globais, como a crise alimentar e energética ². No entanto, para que sejam viáveis em escala industrial, é essencial a otimização das condições de cultivo , a adaptação de biorrefinarias e a implementação de estratégias avançadas de triagem e engenharia de linhagens ³.
Dentre as abordagens promissoras, destaca-se a redução do tamanho da antena de clorofila , que pode aumentar significativamente a eficiência na conversão de energia solar em biomassa , maximizando o rendimento dos cultivos fototróficos⁴.
Triagem e Otimização de Cultivos de Microalgas
A triagem eficiente de linhagens e a otimização das condições de cultivo são etapas fundamentais para o desenvolvimento de processos escaláveis. Dispositivos baseados em microrreservatórios são amplamente utilizados para cultivo de células microbianas e de mamíferos , permitindo experimentos em alto rendimento ⁵.
Tais sistemas já demonstraram grande potencial no desenvolvimento de bioprocessos para microalgas heterotróficas , acelerando a pesquisa e a otimização de parâmetros críticos⁶. No entanto, cultivos autotróficos e mixotróficos exigem microfotobiorreatores (µPBRs) para a determinação precisa das condições ideais de crescimento . Ainda assim, os sistemas convencionais carecem de avanços, especialmente no que se refere ao controle preciso da iluminação ⁷.
Configuração do BioLector XT para o Cultivo Fototrófico
Para este estudo, o microbioreator BioLector XT foi equipado com um módulo de iluminação avançado , permitindo cultivos fototróficos paralelos em até 48 microrreservatórios . Para garantir um monitoramento contínuo e preciso, foram desenvolvidos módulos de filtro especializados , possibilitando a medição online e não invasiva de variáveis essenciais, como biomassa, concentração de clorofila e pH .
O sistema inclui o Light Array Module (LAM) , projetado para oferecer regimes de iluminação ajustáveis dentro dos espectros fotossintéticos relevantes. Com 16 tipos distintos de LEDs , cada um ajustável individualmente, o LAM proporciona uma flexibilidade espectral otimizada , atingindo irradiâncias máximas próximas de 4000 μmol/m²/s .
Características e Aplicações da Chlorella vulgaris
A microalga Chlorella vulgaris pode crescer sob condições fototróficas, heterotróficas e mixotróficas ¹³. Atualmente, é um dos gêneros de microalgas mais comercializados no mundo , com uma produção anual estimada em 5.000 toneladas de biomassa ¹⁴.
Essa espécie apresenta altas taxas de crescimento sob diferentes condições de cultivo e tem sido amplamente estudada devido ao seu potencial na produção de compostos bioquímicos com aplicações industriais¹⁵. Seu elevado teor proteico , com um perfil de aminoácidos alinhado às recomendações da Organização Mundial da Saúde (OMS) para nutrição humana, torna-a um ingrediente promissor para os setores alimentício e de nutrição animal ¹⁵.
Além disso, sob condições de estresse , C. vulgaris acumula ácidos graxos de cadeia C16 e C18¹⁶,¹⁷, ampliando seu potencial para a produção de biocombustíveis , especialmente em processos associados ao tratamento de águas residuais ¹⁵.

Figura 1 - O microbioreator BioLector XT com o LAM.
Cultivo Fotoautotrófico no BioLector XT
Para demonstrar a viabilidade do cultivo fotoautotrófico de C. vulgaris , este estudo utilizou o microbioreator BioLector XT , equipado com o módulo de iluminação LAM (Light Array Module) . Além disso, foram desenvolvidos e validados módulos de filtro especializados para o monitoramento online de parâmetros essenciais do cultivo.
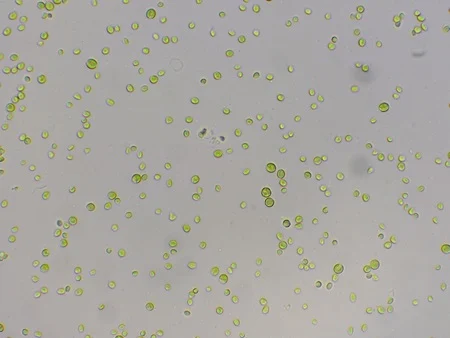
Figura 2 - Chlorella vulgaris cultivada fotoautotróficamente no microbioreator BioLector XT.
Métodos
Desenvolvimento dos Módulos de Filtro
Diversos módulos de filtro foram projetados e testados para o monitoramento online de parâmetros críticos no cultivo fototrófico.
Medição de Biomassa
Para a determinação da biomassa com dispersão de luz¹⁸, foram desenvolvidos módulos de filtro ajustados para operar fora do espectro de absorção da clorofila (>700 nm), evitando interferências pigmentares ¹⁹. Esses módulos foram calibrados utilizando uma série de diluição de Chlorella vulgaris .
Medição do Teor de Clorofila
A fluorescência da clorofila foi utilizada para quantificar concentrações de clorofila em tempo real . Para isso, padrões de clorofila a e b (Sigma-Aldrich) foram dissolvidos em DMSO, e vários módulos de filtro foram testados com séries de diluição de clorofila a e b . Além disso, foi realizada uma calibração da fluorescência da clorofila em relação à biomassa .
Medição do pH
A medição de pH por optodes ²⁰ não pode ser aplicada sob iluminação contínua , devido à sua susceptibilidade ao fotobranqueamento . Como alternativa, utilizou-se o indicador fluorescente solúvel 8-hidroxipireno-1,3,6-trissulfônico trisódico (HPTS) para determinação óptica do pH²¹,²².
Para essa abordagem, dois módulos foram projetados, pois a determinação do pH via HPTS requer medição ratiométrica .
A fluorescência do HPTS em 520 nm varia de acordo com o pH, sendo excitada em 405 e 455 nm , respectivamente. A relação de intensidade (IR) (Eq. 1) é estável no intervalo de pH 0 a 14 ²¹, mas os valores exatos só podem ser calculados após calibração prévia ²². O ajuste dos resultados da calibração à equação de Boltzmann permite a determinação dos parâmetros pH₀, dpH, IR,min e IR,max (Eq. 2)²³.
Com os módulos de filtro projetados , foram geradas curvas de calibração para avaliar o potencial da determinação de pH via HPTS no microbioreator BioLector XT . Além disso, a susceptibilidade dessa técnica ao fotobranqueamento foi testada sob condições típicas de cultivo fototrófico .
Microalga Chlorella vulgaris
A cepa axênica de Chlorella vulgaris utilizada no estudo foi obtida da Culture Collection of Algae da Universidade de Göttingen (SAG Strain Number 211-11b).
Meio de Cultivo
As culturas foram cultivadas em um meio modificado Bold’s Basal Medium (enBBM) , ajustado para um pH de 6,5 ²⁴-²⁷.
A composição do meio incluiu:
-
9,76 g/L MES buffer
-
1,5 g/L NaNO₃
-
0,6 g/L K₂HPO₄
-
1,4 g/L KH₂PO₄
-
187,5 mg/L MgSO₄ · 7 H₂O
-
6,25 mg/L NaCl
-
125 mg/L CaCl₂ · 2 H₂O
-
9,96 mg/L FeSO₄ · 7 H₂O
-
3,68 mg/L H₂SO₄
-
100 mg/L Na₂EDTA · 2 H₂O
-
62 mg/L KOH
-
10 mg/L penicilina G sódica
-
20 mL/L solução de oligoelementos
A solução de oligoelementos foi composta por:
-
17,64 mg/L ZnSO₄ · 7 H₂O
-
2,88 mg/L MnCl₂ · 4 H₂O
-
2,4 mg/L Na₂MoO₄ · 2 H₂O
-
3,14 mg/L CuSO₄ · 5 H₂O
-
0,94 mg/L CoSO₄ · 7 H₂O
-
22,8 mg/L H₃BO₃
Para os cultivos no microbioreator BioLector XT , foi adicionada ao meio uma solução estoque de HPTS , resultando em uma concentração final de 0,1 mg/L .
Cultivo em Frascos Agitados
Os pré-cultivos foram mantidos em frascos agitados , incubados a 25 °C e 180 rpm , com um diâmetro de agitação de 50 mm .
Para garantir o crescimento fototrófico , foi instalado um módulo de LED em uma das laterais da câmara de incubação, enquanto tampões de algodão permitiram a troca gasosa entre o meio e a atmosfera.
O módulo continha oito tiras de LED (LUMITRONIX LED-Technik GmbH) dispostas em paralelo . A irradiância foi ajustada para 200 μmol/m²/s , igualando a irradiância usada no microbioreator BioLector XT .
Cultivo no Microbioreator BioLector XT
O cultivo fototrófico foi realizado em microplacas Flowerplate (M2P-MTP-48-B, m2p-labs , agora parte da Beckman Coulter Life Sciences )²⁸, com uma concentração inicial de 5,5 × 10⁶ células/mL e volume de enchimento de 1 mL .
A microplaca foi selada com uma folha de vedação permeável a gases (MTP-F-GPRS-48-10), permitindo a troca de CO₂ e O₂ durante a fotossíntese .
O módulo de iluminação foi ajustado para fornecer um espectro semelhante ao solar , variando de 400 a 700 nm , com uma densidade de fluxo de fótons de aproximadamente 200 μmol/m²/s ( Figura 3 ).
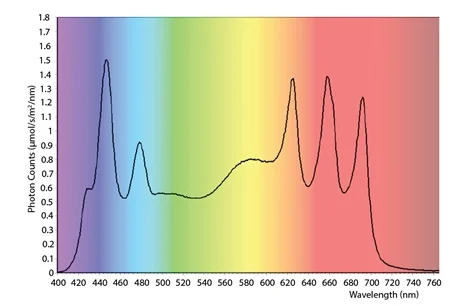
Figura 3 - Espectro de iluminação e irradiância ajustados durante o cultivo.
Os parâmetros de cultivo foram estabelecidos como:
-
Velocidade de agitação: 800 rpm
-
Temperatura: 25 °C
-
Umidade relativa: 85%
-
Taxa de aeração: 10 mL/min
-
Composição do gás: Mistura de ar com 2% de CO₂
Resultados
Calibração dos módulos de filtro
Biomassa
Os filtros de biomassa desenvolvidos a 730, 750 e 850 nm apresentaram excelentes resultados de calibração em um intervalo de 0,3 ≤ OD750 ≤ 25, conforme demonstrado na Figura 3 para o módulo de 730 nm. Além disso, nenhuma interferência da clorofila foi detectada nos padrões de clorofila a e b.
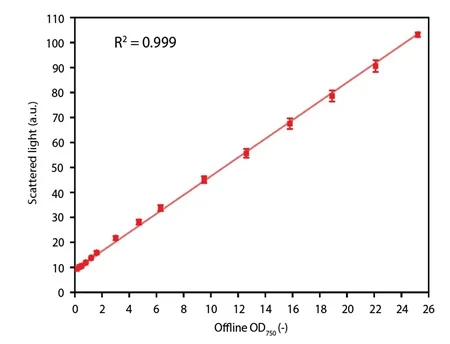
Figura 4 - Calibração de um módulo de filtro de luz espalhada a 730 nm contra uma série de diluições de C. vulgaris .
Clorofila
Os resultados da calibração da clorofila revelaram que os módulos de filtro projetados permitiram a detecção separada e simultânea da clorofila a e b (Figura 5).
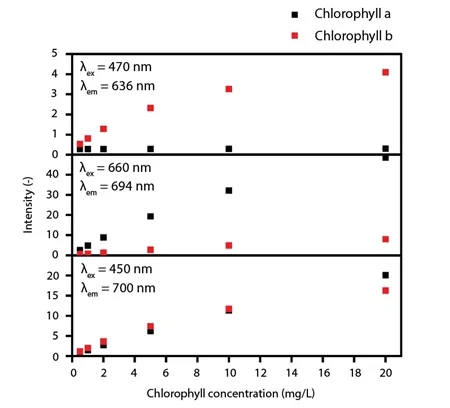
Figura 5 - Calibração dos módulos de filtro de fluorescência da clorofila contra séries de diluição de clorofila a (preto) e clorofila b (vermelho).
A fluorescência da clorofila é frequentemente utilizada para a determinação de biomassa em culturas fototróficas. Assim, foi realizada uma calibração com uma série de biomassa diluída, e uma excelente resolução foi observada em baixas concentrações de biomassa quando um ajuste exponencial decrescente foi aplicado (Figura 6).
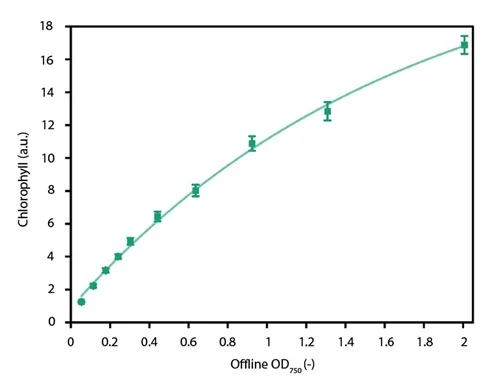
Figura 6 - Calibração do módulo de filtro de clorofila (λex = 450 nm; λem = 700 nm) contra biomassa até OD750 = 2.
Os resultados da calibração confirmam a aplicabilidade dos filtros de fluorescência de clorofila para a determinação precisa da concentração de biomassa, especialmente em baixas concentrações.
pH
Os módulos de filtro de pH foram calibrados a 25, 30, 35 e 40 °C com soluções tampão de pH 5 a 10 (Merck, Darmstadt, DE), contendo 0,1 mg/L de HPTS. Os excelentes resultados de calibração (Figura 7) confirmam que a configuração proposta pode ser usada para uma determinação precisa e online do pH.
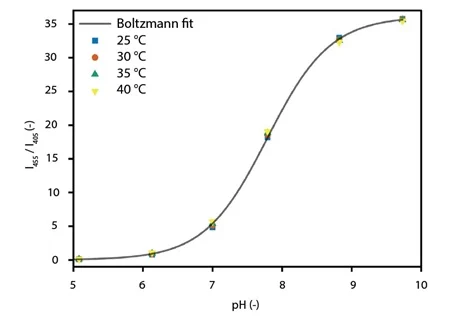
Figura 7 - Calibração da razão de intensidade IR contra o pH, ajustada à equação de Boltzmann.
Para garantir a insensibilidade do método proposto à fotodegradação, foi realizado um experimento no microbioreator BioLector XT sob condições típicas de cultivo, com 200 μmol/m²/s em enBBM sem inóculo (Figura 8).

Figura 8 - Determinação óptica do pH com HPTS em poços triplicados sob condições de cultivo.
A concentração aumentada de CO₂ acidifica rapidamente o meio (~0,05 pH) no início do experimento, mas, posteriormente, os valores medidos permanecem constantes por pelo menos 130 horas (Figura 8). Isso comprova que é possível uma determinação precisa e estável do pH por vários dias sob condições de cultivo e, especialmente, sob iluminação contínua com HPTS.
Cultivo fototrófico paralelo no microbioreator BioLector XT
Em seguida, foi iniciado um cultivo de longo prazo, monitorado online com quatro dos módulos de filtro apresentados: o módulo de luz espalhada a 730 nm, o módulo de fluorescência de clorofila (λex = 450 nm; λem = 700 nm) e ambos os módulos de HPTS para determinação ratiométrica do pH (Figura 9).
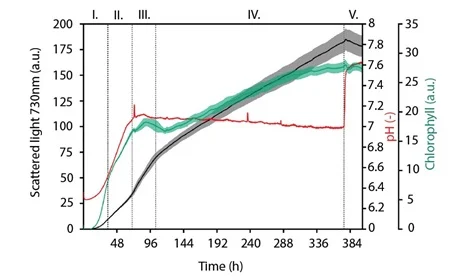
Figura 9 - Luz espalhada, clorofila e pH durante um cultivo de 16 dias no microbioreator BioLector XT em combinação com um módulo de iluminação.
A Figura 9 mostra um aumento contínuo da concentração de biomassa por aproximadamente 16 dias, até que o fornecimento de CO₂ foi interrompido. Cinco fases de crescimento distintas são observadas: iniciando com uma fase lag e uma fase de crescimento exponencial (I.), seguida por três taxas de crescimento linear distintas (II. a IV.), e uma fase de morte (V.) após a depleção de CO₂.
O curso do pH e do sinal da clorofila correlaciona-se com as fases de crescimento observadas. O coeficiente médio de variação do sinal de luz espalhada ao longo do experimento foi de 5,2 %, permitindo cultivos fototróficos paralelos na configuração proposta.
Amostras offline confirmaram a precisão dos sinais online. Após 235 horas – quando foi observada um aumento no pH devido a uma breve exposição ao CO₂ atmosférico – os valores offline de OD750 foram de 40 e o pH offline foi de 7,3, correlacionando-se bem com o pH online de 7,2. No final do experimento, os valores offline de OD750 estavam em torno de 60, indicando um crescimento forte durante o experimento e levando a altas concentrações de biomassa.
Conclusão
Expansão das capacidades do BioLector XT
A adição do Light Array Module representa um avanço significativo para os instrumentos BioLector. Esta aplicação demonstrou vários módulos de filtro capazes de monitorar com precisão os principais parâmetros do cultivo fototrófico: concentração de biomassa, conteúdo de clorofila e pH.
A excelente resolução para a determinação de biomassa em baixas concentrações, obtida com o módulo de filtro de fluorescência de clorofila, complementa a medição de luz espalhada, que é mais precisa em densidades celulares suficientemente altas¹⁸. Além disso, a determinação do pH baseada em HPTS se mostrou uma excelente alternativa às medições com optodos, mesmo sob iluminação contínua.
Cultivo de longo prazo e otimização de parâmetros
O cultivo de longo prazo com Chlorella vulgaris confirmou o potencial do sistema como um fotobiorreator paralelo de alto rendimento em escala microlitro. Além disso, os módulos de filtro desenvolvidos forneceram informações online sobre o crescimento das culturas e revelaram diversas fases de crescimento distintas. Esses resultados oferecem uma plataforma valiosa para a otimização dos cultivos fototróficos de diversas maneiras e aplicações.
O design do módulo de iluminação permite configurar uma ampla faixa espectral e de irradiância sob diferentes regimes de iluminação. Isso possibilita a identificação de condições ideais de iluminação, fator amplamente relatado como influente no crescimento das algas¹²,³¹⁻³⁵.
Outros parâmetros críticos podem ser ajustados para otimizar os cultivos fototróficos, incluindo:
-
Taxa de fluxo e composição do gás: alterações na atmosfera do microbioreator BioLector XT, como enriquecimento com CO₂, resultam em maiores concentrações de biomassa¹⁵,³³.
-
Temperatura³⁶,³⁷.
-
pH¹⁵,³⁴.
-
Salinidade³⁸.
-
Fonte de carbono³⁹⁻⁴¹.
-
Fonte de nitrogênio³³,³⁹.
-
Composição do meio de cultivo⁴².
O BioLector XT permite a otimização de todos esses fatores.
Potencial futuro e aplicações avançadas
O cultivo fed-batch tem sido proposto como uma estratégia para aumentar a produtividade lipídica⁴³. Além disso, o potencial da engenharia genética em algas ainda é pouco explorado devido a restrições regulatórias, mas poderia resultar em:
-
Taxas de crescimento e densidades celulares mais altas.
-
Maior taxa de produção ou título.
-
Maior robustez.
-
Maior eficiência na conversão solar-biomassa e produtividade fotossintética¹,⁸,⁴⁴,⁴⁵.
Todos esses fatores podem ser investigados e otimizados utilizando a combinação proposta do microbioreator BioLector XT e o Light Array Module, acelerando a pesquisa e contribuindo para o aproveitamento do potencial das algas.
References
Hallmann, A., Algae biotechnology–green cell-factories on the rise. Current Biotechnology, 2015. 4(4): p. 389-415.
Tripathi, B.N. and D. Kumar, Prospects and challenges in algal biotechnology. 2017: Springer Singapore.
United Nations, Transforming our World: The 2030 Agenda for Sustainable Development. 2015.
Dos Santos Fernandes de Araujo, R., et al., Brief on algae biomass production. 2019.
Slegers, P.M., et al., Design of Value Chains for Microalgal Biorefinery at Industrial Scale: Process Integration and Techno-Economic Analysis. Frontiers in Bioengineering and Biotechnology, 2020. 8.
Hariskos, I. and C. Posten, Biorefinery of microalgae - opportunities and constraints for different production scenarios. Biotechnology Journal, 2014. 9(6): p. 739-752.
Chisti, Y., Constraints to commercialization of algal fuels. Journal of biotechnology, 2013. 167(3): p. 201-214.
Melis, A., Solar energy conversion efficiencies in photosynthesis: minimizing the chlorophyll antennae to maximize efficiency. Plant science, 2009. 177(4): p. 272-280.
Ojo, E.O., et al., Design and parallelisation of a miniature photobioreactor platform for microalgal culture evaluation and optimisation. Biochemical Engineering Journal, 2015. 103: p. 93-102.
Hillig, F., et al., Bioprocess Development in Single-Use Systems for Heterotrophic Marine Microalgae. Chemie Ingenieur Technik, 2013. 85(1-2): p. 153-161.
Morschett, H., et al., Laboratory-scale photobiotechnology-current trends and future perspectives. FEMS Microbiol Lett, 2018. 365(1).
Kiss, B. and Á. Németh, High-throughput microalgae cultivation with adjustable LED-module applying different colours for Nannochloropsis and Chlorella microcultures. Acta Alimentaria, 2019. 48(1): p. 115-124.
Safi, C., et al., Morphology, composition, production, processing and applications of Chlorella vulgaris: A review. Renewable and Sustainable Energy Reviews, 2014. 35: p. 265-278.
Levasseur, W., P. Perré, and V. Pozzobon, A review of high value-added molecules production by microalgae in light of the classification. Biotechnology Advances, 2020. 41: p. 107545.
Ru, I.T.K., et al., Chlorella vulgaris: a perspective on its potential for combining high biomass with high value bioproducts. Applied Phycology, 2020. 1(1): p. 2-11.
Yeh, K.-L. and J.-S. Chang, Effects of cultivation conditions and media composition on cell growth and lipid productivity of indigenous microalga Chlorella vulgaris ESP-31. Bioresource technology, 2012. 105: p. 120-127.
Maruyama, I., et al., Application of unicellular algae Chlorella vulgaris for the mass-culture of marine rotifer Brachionus, in Live Food in Aquaculture. 1997, Springer. p. 133-138.
m2p-labs GmbH, Baesweiler Germany, The scattered light signal: Calibration of biomass. 2015.
Griffiths, M.J., et al., Interference by pigment in the estimation of microalgal biomass concentration by optical density. Journal of microbiological methods, 2011. 85(2): p. 119-123.
m2p-labs GmbH, Baesweiler Germany, Mode of operation of optical sensors for dissolved oxygen and pH value. 2013.
Wolfbeis, O.S., et al., Fluorimetric analysis. Fresenius’ Zeitschrift für analytische Chemie, 1983. 314(2): p. 119-124.
Kensy, F., et al., Validation of a high-throughput fermentation system based on online monitoring of biomass and fluorescence in continuously shaken microtiter plates. Microbial Cell Factories, 2009. 8(1): p. 31.
Schulte, A., et al., A novel fluorescent pH probe for expression in plants. Plant Methods, 2006. 2: p. 7.
Bischoff, H.W. and H.C. Bold, Some soil algae from Enchanted Rock and related algal species. 1963, Austin, Tex.: University of Texas.
Bold, H.C., The Morphology of Chlamydomonas chlamydogama, Sp. Nov. Bulletin of the Torrey Botanical Club, 1949. 76(2): p. 101-108.
Andersen, R.A., Algal culturing techniques. 2005, Burlington, Mass.: Elsevier/Academic Press.
Morschett, H., W. Wiechert, and M. Oldiges, Accelerated Development of Phototrophic Bioprocesses: A Conceptual Framework. 2017, RWTH Aachen University.
m2p-labs GmbH, Baesweiler Germany, FlowerPlate® Enlighten your Research with our Flowers 2018.
Wiltshire, K.H., et al., The determination of algal biomass (as chlorophyll) in suspended matter from the Elbe estuary and the German Bight: A comparison of high-performance liquid chromatography, delayed fluorescence and prompt fluorescence methods. Journal of Experimental Marine Biology and Ecology, 1998. 222(1): p. 113-131.
Ramaraj, R., D.D. Tsai, and P.H. Chen, Chlorophyll is not accurate measurement for algal biomass. Chiang Mai Journal of Science, 2013. 40(4): p. 547-555.
Carvalho, A.P., et al., Light requirements in microalgal photobioreactors: an overview of biophotonic aspects. Applied Microbiology and Biotechnology, 2011. 89(5): p. 1275-1288.
Johnson, T.J., et al., Photobioreactor cultivation strategies for microalgae and cyanobacteria. Biotechnology Progress, 2018. 34(4): p. 811-827.
Daliry, S., et al., Investigation of optimal condition for Chlorella vulgaris microalgae growth. Global journal of environmental science and management, 2017. 3(2).
Gong, Q., et al., Effects of Light and pH on Cell Density of Chlorella Vulgaris. Energy Procedia, 2014. 61: p. 2012-2015.
Sforza, E., et al., Adjusted Light and Dark Cycles Can Optimize Photosynthetic Efficiency in Algae Growing in Photobioreactors. PLoS ONE, 2012. 7(6): p. e38975.
Serra-Maia, R., et al., Influence of temperature on Chlorella vulgaris growth and mortality rates in a photobioreactor. Algal Research, 2016. 18: p. 352-359.
Converti, A., et al., Effect of temperature and nitrogen concentration on the growth and lipid content of Nannochloropsis oculata and Chlorella vulgaris for biodiesel production. Chemical Engineering and Processing: Process Intensification, 2009. 48(6): p. 1146-1151.
Minhas, A.K., et al., A Review on the Assessment of Stress Conditions for Simultaneous Production of Microalgal Lipids and Carotenoids. Frontiers in Microbiology, 2016. 7.
Kong, W., et al., The characteristics of biomass production, lipid accumulation and chlorophyll biosynthesis of Chlorella vulgaris under mixotrophic cultivation. African Journal of Biotechnology, 2011. 10(55): p. 11620-11630.
Scarsella, M., et al., Study on the optimal growing conditions of Chlorella vulgaris in bubble column photobioreactors. Chem. Eng, 2010. 20: p. 85-90.
Heredia-Arroyo, T., et al., Mixotrophic cultivation of Chlorella vulgaris and its potential application for the oil accumulation from non-sugar materials. Biomass and Bioenergy, 2011. 35(5): p. 2245-2253.
Blair, M.F., B. Kokabian, and V.G. Gude, Light and growth medium effect on Chlorella vulgaris biomass production. Journal of Environmental Chemical Engineering, 2014. 2(1): p. 665-674.
Keil, T., et al., Polymer-based ammonium-limited fed-batch cultivation in shake flasks improves lipid productivity of the microalga Chlorella vulgaris. Bioresour Technol, 2019. 291: p. 121821.
Fayyaz, M., et al., Genetic engineering of microalgae for enhanced biorefinery capabilities. Biotechnology Advances, 2020. 43: p. 107554.
Ng, I.S., et al., Recent Developments on Genetic Engineering of Microalgae for Biofuels and Bio-Based Chemicals. Biotechnology Journal, 2017. 12(10): p. 1600644.

.webp)